
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.
含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.查看答案和解析>>
科目:高中化学 来源: 题型:
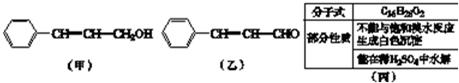
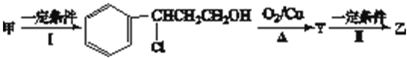 :
:

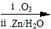 RCHO+R′CHO; 2HCHO
RCHO+R′CHO; 2HCHO 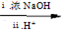 HCOOH+CH3OH
HCOOH+CH3OH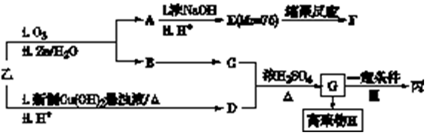


| △ |
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

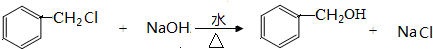

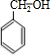
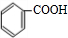 +
+
| 浓硫酸 |
| △ |
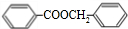 +H2O
+H2O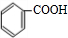 +
+
| 浓硫酸 |
| △ |
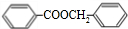 +H2O
+H2O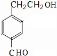

| 溶解性 | 沸点 | |
| A | 微溶于水 | 179.0℃ |
| E | 不溶于水 | 110.8℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com