
【题目】反应N2+3H2![]() 2NH3刚开始时,N2的浓度为3mol/L,H2的浓度5mol/L,3min后测得NH3浓度为0.6mol/L,则此时间内,下列反应速率表示正确的是( )
2NH3刚开始时,N2的浓度为3mol/L,H2的浓度5mol/L,3min后测得NH3浓度为0.6mol/L,则此时间内,下列反应速率表示正确的是( )
A.v(NH3)=0.2mol/(L·min) B.v(N2)=1mol/(L·min)
C.v(H2)=1.67mol/(L·min) D.v(H2)=1.37mol/(L·min)
科目:高中化学 来源: 题型:
【题目】如图,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请回答下列问题:
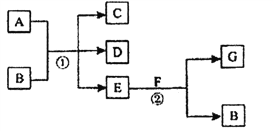
(1)A、G的化学式分别为_______________、________________。
(2)写出A与Fe反应的化学方程式___________________ 。
(3)写出反应②的化学方程式______________________。
(4)己知A是一种重要的化工原料,在工农业生产和生活中有着重要的应用。请根据所学知识回答下列问题。
①将A通入紫色石蕊试液中,观察到的现象是________________;请写出A与水反应的化学方程
式 。
②A与石灰乳反应制得的漂白粉的有效成分是_________(填化学式);该物质在空气中失效的原因______(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从毒韭菜到炸鸡翅、从速溶茶到儿童奶粉,关于食品质量的报道中不断有①“致癌农药”、②“苏丹红”、③“碘元素”、④“亚硝酸盐”、⑤“三聚氰胺”等化学名词出现。业内人士告诉记者,化学性污染正成为危急食品安全的一大“杀手”。上述化学名词所提到的物质中,在某食品添加剂中允许含有但符合限量时不会引起中毒的是( )
A.②③④ B.②③ C.③④ D.只有③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数的值,下列说法正确的是( )
A.含1mol H2SO4的浓硫酸和足量的铜完全反应,转移的电子数为2N A
B.常温常压下5.6g乙烯和环丙烷的混合物中含有的碳原子数为0.4N A
C.在电解精炼铜的过程中,当转移电子数为NA时,阳极质量减少32g
D.某密闭容器盛有0.1 molN2和0.3mol H2在一定条件下充分反应,转移的电子数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德·埃特尔。他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法正确的是
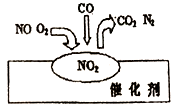
A.NO2是该过程的最终产物
B.NO 和O2必须在催化剂表面才能反应
C.汽车尾气的主要污染成分是CO2和NO
D.该催化转化的总反应方程式为:2NO+O2+4CO![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:①2H2(g)+O2(g)=2H2O(l)ΔH1=-571.6kJmol-1
②2CO(g)+O2(g)=2CO2(g)ΔH2=-566.0kJmol-1
③CO(g)+2H2(g)![]() CH3OH(g)ΔH3=-90.8kJmol-1
CH3OH(g)ΔH3=-90.8kJmol-1
计算甲醇蒸气的燃烧热ΔH= 。
(2)对于可逆反应C(S)+H2O(g)![]() CO(g)+H2(g),平衡常数表达式为 ,能判断该反应一定达到化学平衡状态的依据是 。(填选项编号)
CO(g)+H2(g),平衡常数表达式为 ,能判断该反应一定达到化学平衡状态的依据是 。(填选项编号)
A.容器中气体的平均相对分子质量不随时间而变化
B.v正(H2O)=v逆(H2)
C.容器中气体的密度不随时间而变化
D.容器中总质量不随时间而变化
E.消耗n mol H2的同时消耗n mol CO
(3)某化学兴趣小组探究外界条件对合成甲醇反应的影响。
CO(g)+2H2(g)![]() CH3OH(g)△H=-91kJmol-1
CH3OH(g)△H=-91kJmol-1
①在300℃时,向体积为1L的密闭容器中加入2mol H2和1mol CO,CO和CH3OH(g)的浓度随时间变化如图所示。
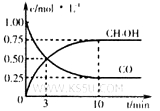
则从反应开始到建立平衡,v(H2)为 ;
②在其它条件不变时,只改变其中的一个条件,该小组同学根据实验绘制如下图像,其中与事实相符的是 。(填序号)
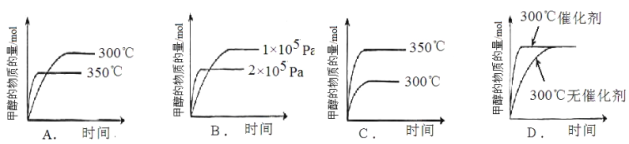
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4.3gNa,Na2O,Na2O2的混合物与足量水反应,在标准状况下得到672ml混合气体将该混合气体通过放电恰好反应,则原混合物中Na、Na2O、Na2O2的物质的量之比
A.1:2:1 B.1:1:1 C.1:3:1 D.4:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大。A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,D元素的价电子数是其余电子数的一半,C与B同主族,A与F同主族,D与E同族。回答下列问题:
(1)A、B、C的第一电离能由大到小的顺序为_______________(用元素符号表示)。
(2)B与C形成的二元化合物中,属于非极性分子的是________(填化学式),该分子中心原子的杂化轨道类型为_____________。
(3)A、C分别形成的常见的含氧酸分子中,中心原子的价层电子对数为4的酸是______(填化学式,下同),酸根呈平面三角形的酸是________________。
(4)Dn+、Br-、C的最高价含氧酸跟、A的简单氢化物按1:1:1:5形成某配合物,向该配合物的溶液中滴加AgNO3溶液产生淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物中的配体为___________,n值为__________,Dn+的基态电子排布式为____________。
(5)立方EB晶体的结构如图所示,其晶胞边长为apm,列式表示EB晶体的密度为__________g·cm-3(不必计算出结果,阿伏伽德罗常数的值为NA)。人工制备的EB晶体中常存在缺陷:一个E2+空缺,另有两个E2+被两个E3+所取代,其结果晶体仍呈电中性,但化合物中E和B的比值却发生了变化。已知某化合物样品组成E0.96B,该晶体中E3+与E2+的离子个数之比为_____________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com