
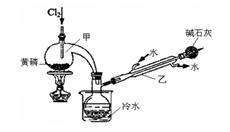
| | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 2PCl3;2P+5Cl2 2PCl3;2P+5Cl2 2PCl5 2PCl5 |
| PCl3 | —112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.Al2(SO4)3 | B.FeSO4 | C.BaCl2 | D.NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A. | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
| B. | 向无色溶液中加硝酸酸化的BaCl2溶液 | 有白色沉淀 | 原溶液中定含SO42- |
| C. | 向Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2CO3的酸性比H2SiO3强 |
| D. | 向某溶液中先加氯水再加KSCN溶液 | 溶液呈血红色 | 原溶液中定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①③ | C.①②④ | D.①③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
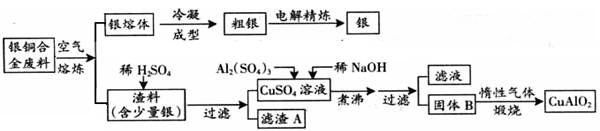
 Cu AlO2 + (系数1也要写).
Cu AlO2 + (系数1也要写).查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.先加入BaCl2溶液,再加入HNO3溶液,产生了白色沉淀,则溶液中一定含有大量的SO42- |
| B.加入足量的CaCl2溶液,产生了白色沉淀,则溶液中一定含有大量的CO32- |
| C.加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32- |
| D.先加适量的硝酸将溶液酸化,再加入AgNO3溶液,产生白色沉淀,则溶液中一定含有大量的Cl— |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com