
【题目】【物质结构与性质】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是____(填元素符号),其中C原子的核外电子排布式为______________;
(2)单质A有两种同素异形体,其中沸点高的是___________(填分子式),原因是_________________;A和B的氢化物所属的晶体类型分为______________和______________;
(3)C和D反应可生成组成比1:3的化合物E,E的立体构型为________________,中心原子的杂化轨道类型___________________;
(4)化合物D2A的立体构型为______________,中心原子的价层电子对数为_______________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_____________________;
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_________,晶胞中A原子的配位数为__________,列式计算晶体F的密度_____________。

【答案】 O 1s22s22p63s23p3 O3 O3相对原子质量较大,范德华力较大 分子晶体 离子晶体 三角锥形 sp3 V形 4 2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl (或2Cl2+Na2CO3 =Cl2O+CO2+2NaCl) Na2O 8 2.27 gcm-3
【解析】A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型,则A是O,B是Na;C、D为同周期元索,C核外电子总数是最外层电子数的3倍,则C是P;D元素最外层有一个未成对电子,所以D是氯元素。
(1)非金属性越强,电负性越大,则四种元素中电负性最大的是O。P的原子序数是15,则根据核外电子排布可知C原子的核外电子排布布式为1s22s22p63s23p3(或[Ne] 3s23p3)。
(2)氧元素有氧气和臭氧两种单质,由于O3相对分子质量较大,范德华力大,所以中沸点高的是O3;A和B的氢化物分别是水和NaH,所属的晶体类型分别为分子晶体和离子晶体。
(3)C和D反应可生成组成比为1:3的化合物E,即E是PCl3,其中P含有一对孤对电子,其价层电子对数是4,所以E的立体构型为三角锥形,中心原子的杂化轨道类型为sp3。
(4)化合物Cl2O分子中氧元素含有2对孤对电子,价层电子对数是4,所以立体构型为V形。单质D与湿润的Na2CO3反应可制备D2A,则化学方程式为2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl。
(5)根据晶胞结构可知氧原子的个数=![]() ,Na全部在晶胞中,共计是8个,则F 的化学式为Na2O。以顶点氧原子为中心,与氧原子距离最近的钠原子的个数8个,即晶胞中A 原子的配位数为8。晶体F的密度=
,Na全部在晶胞中,共计是8个,则F 的化学式为Na2O。以顶点氧原子为中心,与氧原子距离最近的钠原子的个数8个,即晶胞中A 原子的配位数为8。晶体F的密度=![]() 。
。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如下(加热和夹持装置等略):已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:

(1)在250 mL三口瓶a中加入70 mL 70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是___________________________。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。 在装置中,仪器b的作用是____________;仪器c的名称是___________,其作用是___________。反应结束后加适量冷水,再分离出苯乙酸粗品。下列仪器中可用于分离苯乙酸粗品的是___________(填标号)。
A分液漏斗 B漏斗 C烧杯 D直形冷凝管 E玻璃棒
(3)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30 min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与2.24 L O2(标准状况)混合后通入水中,气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入100 mL NaOH溶液,此时Cu2+恰好沉淀完全,所用NaOH溶液的浓度是( )
A.1 mol·L-1 B.2 mol·L-1
C.3 mol·L-1 D.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以重要的化工原料A(C2H2)合成有机物E和![]() 的路线如图所示,部分反应条件及产物略去。其中D在一定条件下可被氧化成酮。
的路线如图所示,部分反应条件及产物略去。其中D在一定条件下可被氧化成酮。
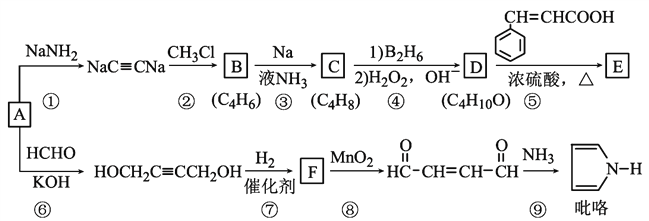
回答下列问题:
(1)B的系统命名是______;已知C是顺式产物,则C的结构简式为_______________。
(2)⑤的反应类型是_________________,E含有的官能团的名称是________________。
(3)反应⑧产物与新制Cu(OH)2的化学方程式为____________________。
(4)符合下列条件肉桂酸(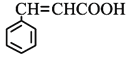 )的同分异构体共____种,分子中含有苯环和碳碳双键,能够发生银镜反应,遇FeCl3溶液显紫色,写出其中核磁共振氢谱图有六组峰,且峰面积之比为1:1:1:1:2:2的结构简式____________________
)的同分异构体共____种,分子中含有苯环和碳碳双键,能够发生银镜反应,遇FeCl3溶液显紫色,写出其中核磁共振氢谱图有六组峰,且峰面积之比为1:1:1:1:2:2的结构简式____________________
(5)参照上述合成路线,设计一条由丙炔和甲醛为起始原料制备![]() 的合成路线__________________________。
的合成路线__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素X所形成的分子X2共有3种,其相对分子质量依次为158、160、162,其三种分子的物质的量之比是7:10:7则下列结论正确的是( )
A. X有三种同位素
B. 其中一种同位素的原子质量数为81
C. 质量数为79的同位素,其原子质量分数为50%
D. X2的平均相对分子质量为159
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2016·江苏化学,14,4分)H2C2O4为二元弱酸。20 ℃时,配制一组c(H2C2O4)+c(HC2O![]() )+c(C2O
)+c(C2O![]() )=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是(双选)( )
)=0.100 mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是(双选)( )

A.pH=2.5的溶液中:c(H2C2O4)+c(C2O![]() )>c(HC2O
)>c(HC2O![]() )
)
B.c(Na+)=0.100 mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O![]() )
)
C.c(HC2O![]() )=c(C2O
)=c(C2O![]() )的溶液中:c(Na+)>0.100 mol·L-1+c(HC2O
)的溶液中:c(Na+)>0.100 mol·L-1+c(HC2O![]() )
)
D.pH=7.0的溶液中:c(Na+)>2c(C2O![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.芳香烃的获取主要来自煤的干馏和对石油分馏产品的催化重整
B.正丁烷转化为异丁烷一定有能量变化
C.石油的催化裂化主要目的是提高轻质液体燃料的产量尤其是汽油的产量
D.石油的常压分馏能得到润滑油、石蜡等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com