
| A£® | øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2+3H2?2NH3”÷H=-92kJ•mol-1 | |
| B£® | aĒśĻߏĒ¼ÓČė“߻ƼĮŹ±µÄÄÜĮæ±ä»ÆĒśĻß | |
| C£® | ¼ÓČė“߻ƼĮ£¬øĆ»Æѧ·“Ó¦µÄ·“Ó¦ČČøıä | |
| D£® | ŌŚĪĀ¶ČĢå»żŅ»¶ØµÄĢõ¼žĻĀ£¬ĶØČė1mol N2ŗĶ3 mol H2·“Ó¦ŗó·Å³öµÄČČĮæĪŖ69kJ£¬ŌņN2µÄ×Ŗ»ÆĀŹĪŖ75% |
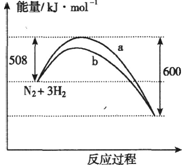
·ÖĪö A£®ÓÉĶ¼æÉÖŖĪŖ·ÅČČ·“Ó¦£¬ČČ»Æѧ·½³ĢŹ½ŠčŅŖ×¢Ć÷ĪļÖŹµÄדĢ¬£¬ĒŅĪļÖŹµÄĮæÓėČČĮæ³ÉÕż±Č£»
B£®“߻ƼĮ½µµĶ·“Ó¦ĖłŠčµÄ»ī»ÆÄÜ£»
C£®“߻ƼĮ²»øÄ±äŹ¼ÖÕĢ¬£»
D£®·Å³öµÄČČĮæĪŖ69kJ£¬æÉÖŖ²Ī¼Ó·“Ó¦µÄµŖĘųĪŖ$\frac{69kJ}{92kJ/mol}$=0.75mol£®
½ā“š ½ā£ŗA£®ÓÉĶ¼æÉÖŖĪŖ·ÅČČ·“Ó¦£¬ČČ»Æѧ·½³ĢŹ½ŠčŅŖ×¢Ć÷ĪļÖŹµÄדĢ¬£¬ĒŅĪļÖŹµÄĮæÓėČČĮæ³ÉÕż±Č£¬ŌņČČ»Æѧ·½³ĢŹ½ĪŖN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92kJ•mol-1£¬¹ŹA“ķĪó£»
B£®“߻ƼĮ½µµĶ·“Ó¦ĖłŠčµÄ»ī»ÆÄÜ£¬ŌņĒśĻßbŹĒ¼ÓČė“߻ƼĮŹ±µÄÄÜĮæ±ä»ÆĒśĻߣ¬¹ŹB“ķĪó£»
C£®“߻ƼĮ²»øÄ±äŹ¼ÖÕĢ¬£¬Ōņ¼Ó“߻ƼĮ£¬·“Ó¦ČČ²»±ä£¬¹ŹC“ķĪó£»
D£®·Å³öµÄČČĮæĪŖ69kJ£¬æÉÖŖ²Ī¼Ó·“Ó¦µÄµŖĘųĪŖ$\frac{69kJ}{92kJ/mol}$=0.75mol£¬ŌņN2µÄ×Ŗ»ÆĀŹĪŖ$\frac{0.75mol}{1mol}$”Į100%=75%£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģā漲鷓ӦČČÓėģŹ±ä£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĶ¼ÖŠÄÜĮæ±ä»Æ”¢ČČ»Æѧ·½³ĢŹ½µÄŹéŠ“”¢ĪļÖŹµÄĮæÓėČČĮæµÄ¹ŲĻµĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāŃ”ĻīCĪŖŅדķµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ģŗĻĪļ£ŗ²ŻÄ¾»Ņ”¢ĘÆ°×·Ū”¢Ė®²£Į§”¢Ė®Ņų | |
| B£® | »ÆŗĻĪļ£ŗ“æ¼ī”¢ÉÕ¼ī”¢Š”ĖÕ“ņ”¢Ź³“× | |
| C£® | µē½āÖŹ£ŗĆ÷·Æ”¢ŹÆøą”¢±ł“×Ėį”¢ĮņĖį±µ | |
| D£® | Ķ¬ĖŲŅģŠĪĢå£ŗ½šøÕŹÆ”¢ŹÆÄ«”¢C60”¢CO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | X | Y | Z |
| A | Cu | HNO3 | Fe£ØNO3£©3 |
| B | FeCl3 | Zn | NaHCO3 |
| C | O2 | NH3 | SO2 |
| D | NH4Al£ØSO4£©2 | Ba£ØNO3£©2 | NaOH |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 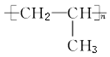 | B£® | 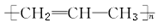 | ||
| C£® | 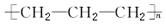 | D£® | 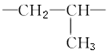 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2 | B£® | CO | C£® | CH3COOH | D£® | C12H22O11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | -332 | B£® | -118 | C£® | 350 | D£® | 130 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬Ļņ100gNaOH±„ŗĶČÜŅŗÖŠ¼ÓČė0.39gNa2O2¹ĢĢ壬»Öø“µ½³£ĪĀ£¬NaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČŅ»¶Ø²»±ä | |
| B£® | ĻņŅ»ŗćČŻČŻĘ÷ÖŠ³äČėlmolN2ŗĶlmolH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦²¢“ļµ½Ę½ŗā£®ÉżĪĀ£¬ŌŁ“Ī“ļµ½Ę½ŗāדĢ¬£¬N2µÄĢå»ż·ÖŹżŅ»¶Ø²»±ä | |
| C£® | Ļņ50mL0.55mol/LµÄNaOHČÜŅŗÖŠ¼ÓČė50mL0.50mol/LµÄĻ”ŃĪĖį£¬²ā¶ØÖŠŗĶČČ£¬¼ĢŠų¼ÓČė6mLµČÅØ¶ČµÄĻ”ŃĪĖį£¬²ā¶ØµÄÖŠŗĶČČŅ»¶Ø²»±ä | |
| D£® | ½«2.3gNaĶ¶Čė100mLĖ®ÖŠ£¬²śÉśH2£¬ČōŌŚ·“Ó¦Ē°ĻņĖ®ÖŠ¼ÓČė100 mLĆŗÓĶ£¬Ōņ²śÉśH2µÄĖŁĀŹŅ»¶Ø²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| H2£Øg£© | Br2£Øg£© | HBr£Øg£© | |
| 1mol·Ö×ÓÖŠµÄ»Æѧ¼ü¶Ļ ĮŃŹ±ŠčŅŖĪüŹÕµÄÄÜĮæ/kJ | 436 | 230 | 369 |
| A£® | 404 | B£® | 72 | C£® | 230 | D£® | 200 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 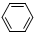 +HNO3$”ś_{”÷}^{ÅØĮņĖį}$ +HNO3$”ś_{”÷}^{ÅØĮņĖį}$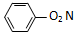 +H2O +H2O | |
| B£® | CH2ØTCH2+H2O$\stackrel{“߻ƼĮ}{”ś}$CH3CH2OH | |
| C£® | 2CH3CHO+O2 $”ś_{¼ÓČČ}^{“߻ƼĮ}$2CH3COOH | |
| D£® | CH4+Cl2$\stackrel{¹āÕÕ}{”ś}$CH3Cl+HCl |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com