
分析 当硫离子浓度较高时,HgS与硫离子能形成[HgS2]2-配离子,据此解答即可.
解答 解:因为在Na2S和NaOH的混合溶液中,溶液为强碱性,S2-水解程度小,即硫离子浓度较大,硫离子能与HgS生成了[HgS2]2-配离子,而使HgS溶解,而在(NH4)2S和NH3•H2O的混合溶液中S2-离子水解程度较大,硫离子浓度低不能生成[HgS2]2-,所以HgS不溶,
故答案为:HgS在Na2S和NaOH的混合溶液中形成配合物,促进了HgS的溶解,而在(NH4)2S和NH3•H2O中不能形成配合物.
点评 本题主要考查的是难溶电解质的溶解平衡与配合物的知识,利用弱根离子的水解是解决本题的关键,难度稍大.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{b{N}_{A}}$ | B. | $\frac{b}{a}$NA | C. | $\frac{a}{b}$ NA | D. | $\frac{b}{a{N}_{A}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
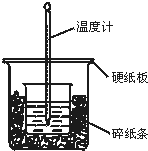 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何晶体中,若含有阳离子也一定含有阴离子 | |
| B. | 原子晶体中只含有共价键 | |
| C. | 离子晶体中只含有离子键 | |
| D. | 分子晶体中只存在分子间作用力,不含化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
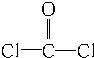 和双酚A:
和双酚A: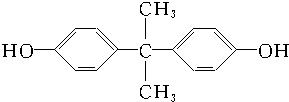 缩聚而成,其反应方程式为
缩聚而成,其反应方程式为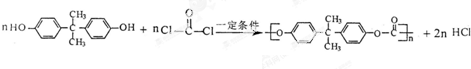 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
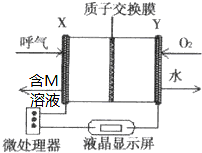 查处酒后驾驶所采用的“便携式乙醇测量仪”,以燃料电池为工作原理,如图,两电极材料均为Pt.理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为M,其中一个电极的反应式为:CH3CH2OH-2e-→M+2H+.下列说法中正确的是( )
查处酒后驾驶所采用的“便携式乙醇测量仪”,以燃料电池为工作原理,如图,两电极材料均为Pt.理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为M,其中一个电极的反应式为:CH3CH2OH-2e-→M+2H+.下列说法中正确的是( )| A. | 电池内部H+向X极移动 | |
| B. | 另一极Y极的电极反应式为:O2+4e-+2H2O=4OH- | |
| C. | 乙醇在X极上发生还原反应,电子经过外电路流向Y极 | |
| D. | 电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com