
| A. | 1.4 g | B. | 15.4 g | C. | 4.4 g | D. | 12.4 g |
分析 根据反应中生成水的质量可确定乙醇的物质的量,进而求出碳原子的物质的量,同时也是CO2和CO的物质的量和,分别设出二氧化碳、一氧化碳的物质的量,分别根据质量、物质的量列式计算即可.
解答 解:设乙醇的物质的量为x,
由C2H5OH~3H2O
1mol 54g
x 10.8g
则:$\frac{1mol}{x}$=$\frac{54g}{10.8g}$,
解得:x=0.2mol,
由乙醇的分子式可知:n(CO2)+n(CO)=0.2mol×2=0.4mol,
则m(CO2)+m(CO)=27.6g-10.8g=16.8g,
设产物中含有xmol二氧化碳、ymolCO,
则:①44x+28y=16.8g,②x+y=0.4,
联立①②解得:x=0.35、y=0.05,
所以二氧化碳的质量为:44g/mol×0.35mol=15.4g,
故选B.
点评 本题考查化学反应方程式的计算,题目难度中等,把握水的质量及CO、CO2的质量关系及守恒法计算为解答的关键,试题侧重对学生的分析与计算能力的考查.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:选择题
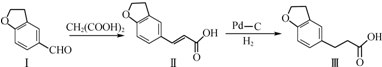
| A. | 与化合物Ⅰ互为同分异构体,且分子中含有2个醛基的芳香族化合物有9种 | |
| B. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| C. | 化合物Ⅱ中共含有4种官能团 | |
| D. | 可用溴水区分化合物Ⅱ和化合物Ⅲ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 服进肠胃的药剂根本不会直接进入人的膀胱中,Cu(OH)2悬浊液无法与葡萄糖作用 | |
| B. | 所用药剂具有毒性(含重金属元素Cu)和强腐蚀性(含NaOH),不能内服 | |
| C. | 该同学设计是正确的,但由于体温达不到令Cu(OH)2悬浊液与葡萄糖反应的温度,故检验不会成功 | |
| D. | 由于人们吃入的淀粉在体内也能水解成葡萄糖,会干扰检验的现象,检验应空腹进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电池工作时,MnO2失去电子 | |
| B. | 电池工作时,电子由锌经外电路流向MnO2 | |
| C. | 从反应方程式来看,不使用氢氧化钾,也不影响电流大小 | |
| D. | 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢和铁 | B. | 金刚石和石墨 | C. | 红磷和白磷 | D. | 氧气和臭氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
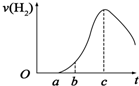 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间(单位:秒)的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间(单位:秒)的关系可用如图曲线来表示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
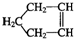 可简写为
可简写为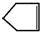 .降冰片烯的分子结构可表示为:
.降冰片烯的分子结构可表示为: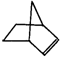
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com