
| A、原子半径:A<B<C |
| B、A的氢化物稳定性大于C的氢化物稳定性 |
| C、三种元素的最高价氧化物对应水化物均可由化合反应得到 |
| D、高温下,A单质能置换出C单质 |
| 10-2 |
| 2 |
| 10-2 |
| 2 |


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.10 | B、0.20 |
| C、0.30 | D、0.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CN-可以和稀硫酸反应生成HCN |
| B、CN-可被I2氧化成(CN)2 |
| C、在水溶液中(CN)2可被F-还原 |
D、HCN的电子式为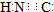 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO32-+H2O?HCO3-+OH-用热的纯碱溶液清洗油污 |
| B、Al3++3H2O?Al(OH)3+3H+明矾净水 |
| C、TiCl4+(x+2)H2O(过量)═TiO2?xH2O↓+4HCl 制备TiO2纳米粉 |
| D、SnCl2+H2O═Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
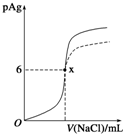 已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )
已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )| A、原AgNO3溶液的物质的量浓度为0.1 mol?L-1 |
| B、图中x点的坐标为(100,6) |
| C、图中x点表示溶液中Ag+被恰好完全沉淀 |
| D、把0.1 mol?L-1的NaCl换成0.1mol?L-1NaI则图象在终点后变为虚线部分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用激光笔检验淀粉溶液的丁达尔现象 |
| B、在容量瓶中加一定体积的水,再加入氢氧化钠晶体配制准确浓度的氢氧化钠溶液 |
| C、加入适量铜粉除去Cu(NO3)2溶液中的AgNO3杂质 |
| D、用食醋除去暖瓶中的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=7的溶液中:K+、Fe3+、Cl-、NO32- |
| B、强酸性溶液中:Cu2+、ClO-、Cl-、Ba2+ |
| C、0.1mol?L-1 的NaHCO3溶液中:K+、Al3+、Fe3+、NO3- |
| D、由水电离出的c(H+)=10-13mol?L-1的溶液中:Al3+、K+、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com