

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
①反应I的平衡常数表达式为K=________________________
②下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH2________0,ΔS______0 (填“>”、“=”或“<”=)。
③对于反应II,若容器容积不变,下列措施可增加甲醇产率的是__________。
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.按原比例再充入 CO和 H2
④某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为_______(从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1275.6 kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g) ΔH =-566.0 kJ·mol-1
③ H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式____________________。
(3)某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置。

①该电池中OH-向_______极移动(填“正”或“负”)
②该电池负极的电极反应为_________________________。
③用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为_______________,电解过程中收集到标准状况下的气体体积为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g)CH3OH(g) ΔH2
①反应I的平衡常数表达式为K=________________________
②下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH2________0,ΔS______0 (填“>”、“=”或“<”=)。
③对于反应II,若容器容积不变,下列措施可增加甲醇产率的是__________。
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.按原比例再充入 CO和 H2
④某温度下,将2mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为________,此时的温度为_______(从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1275.6 kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g) ΔH =-566.0 kJ·mol-1
③ H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式____________________。
(3)某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置。
①该电池中OH-向_______极移动(填“正”或“负”)
②该电池负极的电极反应为_________________________。
③用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为_______________,电解过程中收集到标准状况下的气体体积为__________________。
查看答案和解析>>
科目:高中化学 来源:2011届浙江省温州中学高三上学期期中考试化学卷 题型:填空题
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
反应II:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
①反应I的平衡常数表达式为K=________________________
②下表所列数据是反应Ⅱ在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| A.升高温度 | B.将CH3OH(g)从体系中分离 |
| C.充入He,使体系总压强增大 | D.按原比例再充入 CO和 H2 |

查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省兖州市高三上学期入学检测化学试卷 题型:填空题
(10分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物。请回答:
(1)C和E两种元素相比较,原子得电子能力较强的是(填元素名称) ,以下三种说法中,可以验证该结论的是(填写编号) ;
A.比较这两种元素的常见单质的沸点
B.二者形成的化合物中,C元素的原子显负价
C.比较这两种元素的气态氢化物的稳定性
(2)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为 。
(3)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2LO2,消耗该化合物的质量为___________。
(4)B2A4是一种可燃性液体,B2A4—空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2。用该燃料电池电解足量的饱和食盐水,如下图所示:
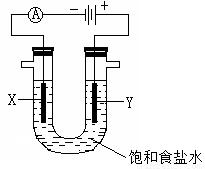
电解装置内发生反应的离子方程式为______________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com