
分析 在25℃时,0.05mol/L H2SO4溶液中c(H+)=0.05mol/L×2=0.1mol/L,该溶液稀释100倍后,氢离子浓度是原来的$\frac{1}{100}$,pH=-lgc(H+),据此分析解答.
解答 解:在25℃时,0.05mol/L H2SO4溶液中c(H+)=0.05mol/L×2=0.1mol/L,pH=-lgc(H+)=-lg0.1=1;该溶液稀释100倍后,氢离子浓度是原来的$\frac{1}{100}$,为0.001mol/L,pH=-lgc(H+)=-lg0.001=3,
故答案为:1;3.
点评 本题考查pH的有关计算,为高频考点,侧重考查学生分析计算能力,注意硫酸是二元酸,氢离子浓度是硫酸二倍,注意:如果溶液稀释至接近中性时要考虑水的电离,题目难度不大.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 产生丁达尔现象 | B. | 胶体是混合物 | ||
| C. | 分散质粒子直径在1nm~100nm之间 | D. | 胶体的分散剂为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾用于净水与K+、Al3+的水解有关 | |
| B. | 配制FeCl3溶液时,为了抑制Fe3+的水解,常加入少量稀硫酸 | |
| C. | 常常用排饱和食盐水的方法收集氯气,可以避免氯气溶于水而损失 | |
| D. | 将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL,10.6g | B. | 100mL,10.1g | C. | 500mL,10.1g | D. | 500mL,10.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时的速率:甲<乙 | |
| B. | 反应所需时间:甲>乙 | |
| C. | 反应开始前,酸的物质的量浓度:甲=乙 | |
| D. | 若使两酸溶液PH都等于5,则加水的体积:甲=乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L溶液中Cl-离子浓度为0.2mol•L-1 | |
| B. | 1L溶液中Cl-离子总数为0.2NA | |
| C. | 1L溶液中Ba2+离子浓度为0.2mol•L-1 | |
| D. | 1L溶液中Ba2+和Cl-离子总数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (R、R’代表烃基)
(R、R’代表烃基) .
. .
. 与足量NaOH溶液反应时,最多消耗4mol NaOH
与足量NaOH溶液反应时,最多消耗4mol NaOH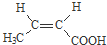 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 放入0.2mol SO2、0.1molO2、0.1mol SO3,达到平衡时SO3必小于amol | |
| B. | 放入0.2mol SO2、0.1molO2、0.2mol SO3,达到平衡时SO3必大于amol | |
| C. | 放入0.4mol SO2、0.1molO2,达到平衡时SO3会等于0.4amol | |
| D. | 放入0.2mol SO2、0.1molO2,达到平衡时SO3必小于amol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 0.01mol/L KIO3溶液的体积/mL | Na2SO3溶液的体积/mL | H2O的 体积/mL | 实验温度/℃ | 溶液出现蓝色所需的时间 | |
| 实验1 | 5 | 5 | V1 | 0 | a |
| 实验2 | 5 | 5 | 40 | 25 | b |
| 实验3 | 5 | V2 | 35 | 25 | c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com