
只有阳离子而没有阴离子的晶体是 ( )。
A.金属晶体 B.原子晶体
C.离子晶体 D.分子晶体
科目:高中化学 来源: 题型:

25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s)
体系中c(Pb2+)和c(Sn2+)变化关系如图所示。
下列判断正确的是( )
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
D.25 ℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
蔗糖酯是联合国国际粮农组织和世界卫生组织推荐使用的食品乳化剂。某蔗糖酯可以由蔗糖与硬脂酸乙酯合成,反应如下:
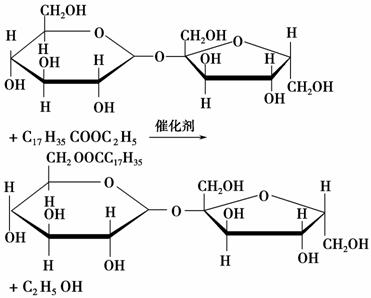
下列说法中正确的是( )。
A.蔗糖分子中含有1个羟基
B.蔗糖酯属于高级脂肪酸的甘油酯
C.合成该蔗糖酯的反应属于取代反应
D.该蔗糖酯在稀硫酸的作用下水解,水解过程中只生成两种产物
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO 、Fe2+、NH
、Fe2+、NH 、H+、H2O,下列叙述正确的是 ( )。
、H+、H2O,下列叙述正确的是 ( )。
A.该反应说明Fe(NO3)2溶液不宜加酸酸化
B.该反应中氧化剂与还原剂物质的量之比为8∶1
C.若有1 mol NO 发生氧化反应,转移电子5 mol
发生氧化反应,转移电子5 mol
D.若将该反应设计成原电池,则负极反应为Fe3++e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属键的叙述中,不正确的是 ( )。
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互
作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所
以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键
无饱和性和方向性
D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动
查看答案和解析>>
科目:高中化学 来源: 题型:
结合金属晶体的结构和性质,回答以下问题:
(1)根据下列叙述,判断一定为金属晶体的是________。
A.由分子间作用力形成,熔点很低
B.由共价键结合形成网状晶体,熔点很高
C.固体有良好的导电性、传热性和延展性
(2)下列关于金属晶体的叙述正确的是________。
A.常温下,金属单质都以金属晶体形式存在
B.金属阳离子与自由电子之间的强烈作用,在一定外力作用下,不因形变
而消失
C.钙的熔、沸点高于钾
D.温度越高,金属的导电性越好
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质既不是同系物又不是同分异构体的是( )
A.软脂酸甘油酯和硬脂酸甘油酯 B.甲酸甲酯和乙酸
C.对甲基苯酚和苯甲醇 D.油酸甘油酯和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.硬脂酸和软脂酸都属于酸,一个是饱和酸,一个是不饱和酸
B.植物油不能使溴的四氯化碳溶液褪色
C.柴油可以在碱性条件下水解
D.可通过反应后的溶液不分层,判断油脂的皂化反应基本完成
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上由 CO2 和 H2 合成气态甲醇的热化学方程式为:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH=-50 kJ·mol-1。下面表示合成甲醇的反应的能量变化示意图,其中正确的是 ( )。
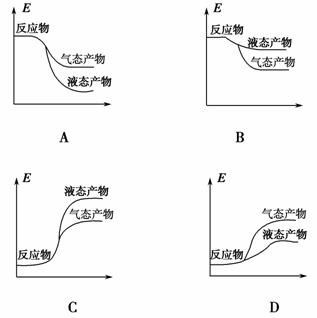
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com