
| A£® | ÄĘŌŚ×ŌČ»½ēÖŠ²»“ęŌŚÓĪĄėĢ¬ | B£® | ÄĘŹĒŅ»ÖÖ°×É«¹ĢĢå | ||
| C£® | ÄĘæÉŅŌ±£“ęŌŚĆŗÓĶÖŠ | D£® | ÄĘ×Å»šŹ±æÉŅŌÓĆĖ®Ćš»š |
·ÖĪö ÄĘŠŌÖŹ»īĘĆ£¬Č¼ÉÕÉś³É¹żŃõ»ÆÄĘ£¬Ņ×ÓėæÕĘųÖŠµÄĖ®”¢ŃõĘų·“Ó¦£¬ŌŚ×ŌČ»½ēÖŠŅŌ»ÆŗĻĢ¬“ęŌŚ£¬ÓėĆŗÓĶ²»·“Ó¦£¬ĒŅĆܶȱČĆŗÓĶ“ó£¬æɱ£“ęŌŚĆŗÓĶÖŠ£®
½ā“š ½ā£ŗA£®Ņ×ÓėæÕĘųÖŠµÄĖ®”¢ŃõĘų·“Ó¦£¬ŌŚ×ŌČ»½ēÖŠŅŌ»ÆŗĻĢ¬“ęŌŚ£¬¹ŹAÕżČ·£»
B£®ÄĘĪŖŅų°×É«¹ĢĢ壬¹ŹB“ķĪó£»
C£®ÓėĆŗÓĶ²»·“Ó¦£¬ĒŅĆܶȱČĆŗÓĶ“ó£¬æɱ£“ęŌŚĆŗÓĶÖŠ£¬¹ŹCÕżČ·£»
D£®ÄĘÓėĖ®¾ēĮŅ·“Ó¦£¬²»ÄÜÓĆĖ®ĘĖĆš£¬¹ŹD“ķĪó£®
¹ŹŃ”AC£®
µćĘĄ ±¾Ģāæ¼²éÄʵĊŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲÓŚĖ«»łµÄ漲飬ӊĄūÓŚÅąŃųѧɜĮ¼ŗƵÄæĘѧĖŲŃų£¬ĢāÄæÄŃ¶Č²»“ó£¬Ń§Ļ°ÖŠ×¢ŅāĻą¹ŲÖŖŹ¶µÄ»żĄŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2H2+O2$\frac{\underline{\;µćČ¼\;}}{\;}$2H2O | B£® | CO2+H2OØTH2CO3 | ||
| C£® | Fe+H2SO4ØTFeSO4+H2”ü | D£® | MgCO3+2HClØT2MgCl2+CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH3·Ö×Ó±ČPH3·Ö×ÓĪČ¶Ø | |
| B£® | Ķس£ĒéæöNH3¼«Ņ×ČÜÓŚĖ® | |
| C£® | ±łµÄĆܶȱČŅŗĢ¬Ė®µÄĆܶȊ” | |
| D£® | ŌŚĻąĶ¬Ģõ¼žĻĀ£¬H2OµÄ·Šµć±ČH2SµÄ·Šµćøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C60ŹĒŅ»ÖÖŠĀŠĶµÄ»ÆŗĻĪļ | B£® | C60ŗĶŹÆÄ«»„ĪŖĶ¬ĖŲŅģŠĪĢå | ||
| C£® | C60ÖŠŹĒŅ»ÖÖĢ¼Ō×Ó | D£® | C60µÄŹ½ĮæŹĒ120 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH3 | B£® | SO2 | C£® | NO2 | D£® | Cl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ħ¶ūŹĒĪļÖŹµÄĮæµÄµ„Ī» | |
| B£® | ĪļÖŹµÄĮæµÄ·ūŗÅŹĒM | |
| C£® | H2µÄĦ¶ūÖŹĮæŹĒ2g | |
| D£® | NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬lmolCl2ŗ¬ÓŠ2NAøöĀČŌ×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
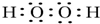 £®W”¢X”¢Y µÄĄė×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖS2-£¾O2-£¾Al3+£ØÓĆĄė×Ó·ūŗÅ»Ų“š£©
£®W”¢X”¢Y µÄĄė×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖS2-£¾O2-£¾Al3+£ØÓĆĄė×Ó·ūŗÅ»Ų“š£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ć¾Ę¬ÓėĻ”ĮņĖįµÄ·“Ó¦ | B£® | Ba£ØOH£©2•8H2OÓėNH4Cl·“Ó¦ | ||
| C£® | ×ĘČȵÄĢæÓėCO2µÄ·“Ó¦ | D£® | ¼×ĶéŌŚŃõĘųÖŠµÄČ¼ÉÕ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £»ŗ¬¼«ŠŌ¹²¼Ū¼üµÄ·Ö×ÓµÄÖŠŠÄŌ×Ó¹ģµĄŌÓ»ÆĄąŠĶsp£»
£»ŗ¬¼«ŠŌ¹²¼Ū¼üµÄ·Ö×ÓµÄÖŠŠÄŌ×Ó¹ģµĄŌÓ»ÆĄąŠĶsp£»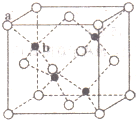
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com