
| A. | CO2+2H2O═CH4+2O2 | B. | NaOH+HCl═NaCl+H2O | ||
| C. | 4Al+3O2+6H2O═4Al(OH)3 | D. | Cu+2HCl═CuCl2+H2↑ |
分析 能设计成原电池的化学反应,必须是能自发进行的氧化还原反应,据此结合化合价变化情况对各选项进行判断.
解答 解:A.反应CO2+2H2O→CH4+2O2不能自发进行,且为吸热反应,无法设计成原电池,故A错误;
B.NaOH+HCl=NaCl+H2O为中和反应,不是氧化还原反应,不能设计成原电池,故B错误;
C.4Al+3O2+6H2O=4Al(OH)3为氧化还原反应,可将化学能转化为电能,故C正确;
D.反应Cu+2HCl=CuCl2+H2↑不能自发进行,无法设计成原电池,故D错误;
故选C.
点评 本题考查了原电池原理,题目难度不大,明确原电池反应类型是解本题关键,该反应必须是“自发进行的”、“放热的”、“氧化还原反应”,这几个特点必须同时具备,缺一不可,试题培养了学生的灵活应用能力.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:解答题
| 滴定序号 | 待测液体积 (mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
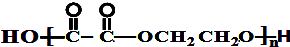 ,可由有机化工原料R和其它有机试剂,通过加成、水解、氧化、缩聚反应得到,则R是( )
,可由有机化工原料R和其它有机试剂,通过加成、水解、氧化、缩聚反应得到,则R是( )| A. | 1-丁烯 | B. | 乙烯 | C. | 1,3-丁二烯 | D. | 2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
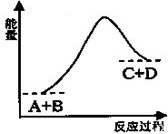
| A. | 只有在加热条件下该反应才能进行 | |
| B. | 该反应是吸热反应 | |
| C. | 反应物的总能量低于生成物的总能量 | |
| D. | 反应中断开化学键吸收的总能量高于形成化学键放出的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同 | |
| B. | 工业利用乙烯水化法制乙醇,是发生了取代反应 | |
| C. | 乙烯在空气中燃烧,发生明亮并带有淡蓝色的火焰 | |
| D. | 水果运输中为延长果实的成熟期,常在车厢里放置浸泡过高锰酸钾溶液的硅藻土 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | |
| B. | 比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| D. | NH4Cl的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:1 | ||
| C. | 该有机物可能为烃 | D. | 此有机物的最简式为CH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com