



 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:填空题
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
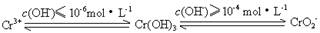
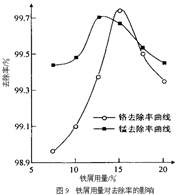
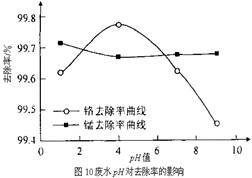
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
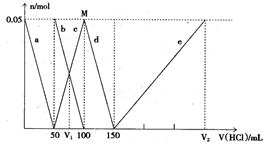
| A.原混合溶液中的CO32-与AlO2—的物质的量之比为1:2 |
| B.V1:V2=l:5 |
| C.M点时生成的CO2为0、05mol |
| D.a曲线表示的离子方程式为:AlO2—+H++H2O=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)配制时,必须使用的仪器有 (填序号),还缺少的仪器是 实验两次用到玻璃棒,其作用分别是 、 。
mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)配制时,必须使用的仪器有 (填序号),还缺少的仪器是 实验两次用到玻璃棒,其作用分别是 、 。 将实验③中的碱性溶液加热,有气体放出,该气体
将实验③中的碱性溶液加热,有气体放出,该气体 能使湿润的红色石蕊试纸变蓝。
能使湿润的红色石蕊试纸变蓝。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCO3— | B.Na+ | C.Ba2+ | D.NO3— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.4mol/L | B.0.3mol/L | C.0.2mol/L | D.0.1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com