
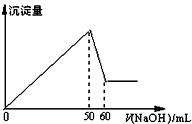
 在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度
在AlCl3和MgCl2的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中AlCl3与MgCl2的物质的量浓度| A. | 1:1 | B. | 3:1 | C. | 1:2 | D. | 2:1 |
分析 在AlCl3和MgCl2的混合溶液中滴加NaOH溶液,生成的沉淀逐渐增加,当沉淀达到最大量后,氢氧化铝沉淀开始溶解,设出氯化铝、氯化镁、NaOH的物质的量浓度,然后根据图象中数据列式计算即可.
解答 解:设氯化铝的物质的量浓度为x,氯化镁的浓度为y,氢氧化钠溶液的浓度为z,原混合液体积为VL,
溶解氢氧化铝的反应为:Al(OH)3+OH-═AlO2-+2H2O,总共消耗了60mL-50mL=10mLNaOH溶液,
则:xV=0.01×z,x=$\frac{0.01z}{V}$,
氯化铝、氯化镁转化成氢氧化铝、氢氧化镁沉淀消耗氢氧化钠的总体积为50mL,
则:3xV+2yV=0.05z,将x=$\frac{0.01z}{V}$带入可得:y=$\frac{0.01z}{V}$,
所以原混合液中AlCl3与MgCl2的物质的量浓度之比为x:y=$\frac{0.01z}{V}$:$\frac{0.01z}{V}$=1:1,
故选A.
点评 本题考查了混合物反应的计算、物质的量浓度的计算,题目难度中等,明确图象中曲线变化的含义为解答关键,注意掌握混合物反应计算的方法与技巧,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论或目的 |
| A | 向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液呈红色 | 红砖中含有氧化铁 |
| B | CO还原Fe2O3得到的黑色固体加入盐酸溶解后再加入KSCN溶液,溶液不显红色 | 黑色固体中没有Fe3O4 |
| C | 取少量Fe(NO3)2试样加水溶解,加稀H2SO4酸化,滴加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经变质 |
| D | 向某溶液中通入Cl2,然后再加入KSCN溶液变红色 | 原溶液中含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 应称取的质量NaOH/g | 应选用容量瓶的规格/ml | 除容量瓶外还需要的其它玻璃仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
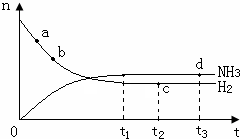 氨气是一种重要的化工原料,大量用于制造尿素、纯碱、铵态氮肥以及硝酸,在有机合成工业中制合成纤维、塑料、染料等.请回答下列问题:
氨气是一种重要的化工原料,大量用于制造尿素、纯碱、铵态氮肥以及硝酸,在有机合成工业中制合成纤维、塑料、染料等.请回答下列问题:| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 23.1 |
| b | 2 | 6 | 0 | 未知(用E表示) |
| 容器 | c(CO2) /mol•L-1 | c(H2) /mol•L-1 | c(CH3OCH3) /mol•L-1 | c(H2O) /mol•L-1 | v (正)和v (逆)比较 |
| 容器I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v (正)=v (逆) |
| 容器II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{77}^{192}$Ir原子核内含有192个质子 | |
| B. | ${\;}_{77}^{192}$Ir 和${\;}_{77}^{191}$Ir互为同位素 | |
| C. | ${\;}_{77}^{192}$Ir原子核内含有77个中子 | |
| D. | ${\;}_{77}^{192}$Ir的电子数为115 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)═2H2O(g),△H=-483.6kJ,则氢气的燃烧热为241.8kJ•mol-1 | |
| B. | 已知OH-(aq)+H+(aq)═H2O(l)△H=-57.3kJ•mol-1,则含40.0gNaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 | |
| C. | 已知2C(s)+2O2(g)═2CO2(g)△H=a;2C(s)+O2(g)═2CO(g),△H=b,则a>b | |
| D. | 已知C(石墨,s)═C(金刚石,s)△H>0,则石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
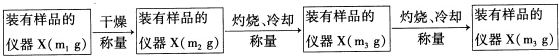
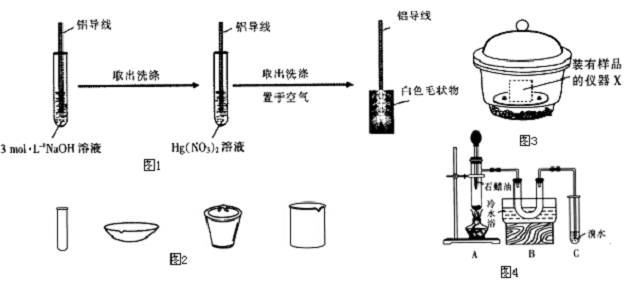
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
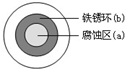
| A. | 液滴中的Cl-由a区向b区迁移 | |
| B. | 液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-→4OH- | |
| C. | 液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 | |
| D. | 若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-→Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com