
1830年,法国化学品制造商库尔曼就提出,氨能跟氧气在铂催化下得到硝酸,其中第一步反应为:4NH3+5O2===4NO+6H2O(各物质均为气态),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol·L-1·min-1]表示,则正确的关系是( )
A.4v(NH3)/5=v(O2) B.5v(O2)/6=v(H2O)
C.2v(NH3)/3=v(H2O) D.4v(O2)/5=v(NO)
科目:高中化学 来源: 题型:
根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l)
ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l)
ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g)
ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2
C.Q3>Q2>Q1 D.Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”和“含氟牙膏”等商品,这里的碘、铁、钙、硒、氟应理解为( )
A.元素 B.单质
C.分子 D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)。下列关于元素R的判断中一定正确的是 ( )。
| I1 | I2 | I3 | I4 | …… | |
| R | 740 | 1 500 | 7 700 | 10 500 |
①R的最高正价为+3价 ②R元素位于元素周期表中第ⅡA族 ③R元素第一电离能大于同周期相邻元素 ④R元素基态原子的电子排布式为1s22s2
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
以下关于化学反应速率的论述中,正确的是( )
A.化学反应速率可用某时刻生成物的物质的量来表示
B.在同一反应中,用反应物或生成物表示的化学反应速率数值是相同的
C.化学反应速率的大小主要取决于外界因素
D.可用单位时间内氢离子物质的量浓度的减少来表示NaOH溶液和盐酸的反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列事实中,什么因素影响了化学反应的速率。
(1)集气瓶中,H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸________。
(2)等质量的大理石块和大理石粉分别与相同浓度的盐酸反应,大理石粉反应快______________________________________。
(3)硫在空气中燃烧发出微弱的淡蓝色火焰,在纯氧中迅速燃烧发出明亮的蓝紫色火焰__________________________。
(4)熔化的KClO3放出气泡很慢,撒入少量MnO2产生气体很快____________。
(5)同浓度、同体积的盐酸中放入同样大小的锌条和镁条,产生气体有快有慢______________________________________。
(6)夏天的食品易霉变,冬天就不易发生该现象___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
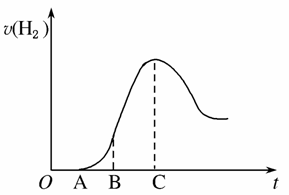
把放置在空气中一段时间的2.0 g铝片投入盛有250 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图所示的坐标曲线来表示,回答下列问题:
(1)曲线OA段不产生氢气的原因是__________________,有关的离子方程式是____________________________。
(2)曲线AB段产生氢气的速率较慢的原因是_____________________________________________________。
(3)曲线BC段产生氢气的速率较快的主要原因是_______________________________________________________。
(4)曲线到C以后,产生氢气的速率逐渐下降的主要原因是_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,将x mL pH=a的稀NaOH溶液与y mL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是( )
A.若x=y,且a+b=14,则pH>7
B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7
D.若x=10y,且a+b=14,则pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g)2SO3(g)反应过程中的能量变化如下图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·mol-1。
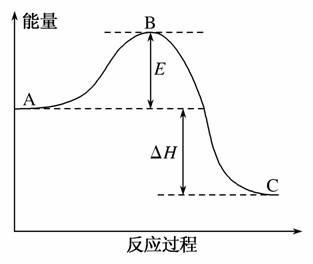
请回答下列问题:
(1)图中A、C分别表示_______________、________________。
(2)图中ΔH=__________ kJ·mol-1。
(3)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3mol SO3(g)的ΔH(要求计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com