
����Ŀ�����ô�������̨���Ǽʿռ䷢����һ���Ǽʷ��ӣ�����ӽṹģ����ͼ��ʾ��ͼ��������֮������ߴ�����ѧ��������������˫���������ȣ���ͬ���Ƶ����ʾ��ͬ��ԭ�ӣ���ͬ���Ƶ����ʾ��ͬ��ԭ�ӣ����Ը������ж���ȷ����
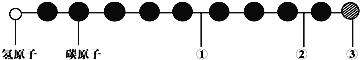
A�������Ļ�ѧ����̼̼˫�� B�������Ļ�ѧ����̼̼����
C�������Ļ�ѧ����̼̼���� D��������ԭ�ӿ�������ԭ�ӻ��ԭ��
���𰸡�B
��������
����������÷���Ϊ�л���л��������̼ԭ���γ���4�����ۼ����������ԭ�ӿ�ʼ�ƶϣ���һ��̼̼��Ϊ̼̼�������ڶ���̼̼��Ϊ������������Ϊ������ͬ�����Ƴ���Ϊ̼̼��������Ϊ̼̼������������������̼Ӧ��Ϊ���������ṹ��ʽΪ��HC��C-C��C-C��C-C��C-C������A�������ļ�Ϊ̼̼������A����B�������ļ�Ϊ̼̼������B��ȷ��C�������ļ�Ϊ̼̼������C����D����ԭ���γɵļ�Ϊ���������Բ�����Ϊ��ԭ�ӻ�����ԭ�ӣ�D������ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[2017����]2017������������ҹ�������Ϊ����Լ��Լ������Դ��������ɫ��Լ�������������Ӧ�ᳫ����
A�������趨�յ��¶Ⱦ����ܵĵ�
B���ƹ�ʹ��һ�������ϴ���ֽ��
C���ٿ�˽�ҳ���˹�����ͨ����
D������Ʒ���к�����װ�ٽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ�����������(NaNO2)��ýȾ����Ư�����ֲĻ�ʴ���������ȴ�������ij��ȤС��������װ���Ʊ�NaNO2��̽��NO��NO2��ijһ��ѧ����(A�м���װ������ȥ)��

��֪����2NO��Na2O2��2NaNO2��
��NO�ܱ�����KMnO4������NO3-��MnO4-����ԭΪMn2��
��ش��������⣺
(1)װ��A������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ__________________��
(2)����ͼ�е�װ���Ʊ�NaNO2��������˳��Ϊ��a��_____________��h(������������Сд��ĸ��ʾ)����ʱ����K1��K2��β���_______________________��
(3)Eװ�÷�����Ӧ�����ӷ���ʽ��________________________��
(4)ͨ���������ϣ�NO2��NO��������Һ��Fe2+������Ӧ��ijͬѧѡ������װ�ò���A��C��E˳�����ӣ�E��װ��FeSO4��Һ����������ʵ��̽����

����ڲ�����Ŀ����__________________�������Cƿ�з����Ļ�ѧ����ʽΪ________________��
ͨ��ʵ����Եó���___________(�NO2��NO�е�һ�ֻ����֡�)����Һ��Fe2+������Ӧʹ��Һ������ɫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ٣����ڱ��е�λ�ã��û�ѧ����ش��������⣺

��1���ٵ�Ԫ�ط���Ϊ______���ڵ�Ԫ�ط���Ϊ______���۵�Ԫ�ط���Ϊ______���ܵ�Ԫ�ط���Ϊ______���ݵ�Ԫ�ط���Ϊ______����Ԫ�ط���Ϊ______���ߵ�Ԫ�ط���Ϊ______�����Ԫ�ط���Ϊ_______
��2����ԭ�ӽṹʾ��ͼΪ_________��
��3�������̬�⻯��Ϊ_____________(�ѧʽ)��
��4���ݶ�Ӧ�ļ�Ļ�ѧʽΪ__________���۵���ۺ�����Ϊ___________�����ѧʽ��
��5���ݡ���Ԫ�صĽ�����ǿ������Ϊ___________�������������С�����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������£�H2O������Ϊxg������y����ԭ�ӣ����ӵ�����Ϊ�� ��
A��18y/x B��9y/x C��18y/ x mol��1 D��9y/x mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ġ���ͼΪN2(g)��O2(g)��Ӧ����NO(g)�����е������仯������˵������ȷ����( )

A��1 mol N2(g)��1 mol O2(g)��Ӧ�ų�������Ϊ180 kJ
B��NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ
C����1 L�������з�����Ӧ��10 min�� N2 ������1 mol�����10 min�ڵ�ƽ����Ӧ����Ϊv(NO)=0.1 mol/(L��min)
D��1 mol N2(g)��1 mol O2(g)�����������2 mol NO(g)���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����ѧ��Ӧ�����Dz���Ҫ�������ʱ仯����Ҫ�о������仯�ͷ�Ӧ������
��1��������һ������Ȼ����ˮ��Ӧ�Ʊ������ķ�Ӧ���䷽��ʽΪ��CH4(g)+ 2H2O(g) ![]() CO2(g)+4H2(g)�÷�Ӧ�����������仯��ͼ��ʾ����÷�ӦΪ______��Ӧ������ȡ����ȡ�����
CO2(g)+4H2(g)�÷�Ӧ�����������仯��ͼ��ʾ����÷�ӦΪ______��Ӧ������ȡ����ȡ�����
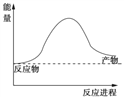
����֪���ƻ�1mol��ѧ����Ҫ���յ��������±���ʾ����÷�Ӧ���ջ�ų�����Ϊ______kJ (�ú�a b c d��ĸ�Ĵ���ʽ��ʾ)��
��ѧ�� | C��H | O��H | C=O | H��H |
����������kJ/mol�� | a | b | c | d |
��2��һ���¶��£���3 molA�����1mol B����ͨ��һ�ݻ��̶�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)��B(g) ![]() xC(g)����Ӧ1minʱ���ʣ��1.8molA��C��Ũ��Ϊ0.4mol/L����1min�ڣ�B��ƽ����Ӧ����Ϊ________��XΪ__________������Ӧ��2min�ﵽƽ�⣬ƽ��ʱC��Ũ��______0.8mol/L������ڡ�����С�ڡ����ڡ���������֪��ƽ��ʱ���������ڻ��������ѹǿΪp�����������ʼѹǿΪp0������p0��p����ʾ��ƽ��ʱ��Ӧ��A��ת����Ϊ__________��
xC(g)����Ӧ1minʱ���ʣ��1.8molA��C��Ũ��Ϊ0.4mol/L����1min�ڣ�B��ƽ����Ӧ����Ϊ________��XΪ__________������Ӧ��2min�ﵽƽ�⣬ƽ��ʱC��Ũ��______0.8mol/L������ڡ�����С�ڡ����ڡ���������֪��ƽ��ʱ���������ڻ��������ѹǿΪp�����������ʼѹǿΪp0������p0��p����ʾ��ƽ��ʱ��Ӧ��A��ת����Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ������ڵ�һ���������ʾ�������й�A��B��C��D��E����Ԫ�ص������У���ȷ���ǣ� ��
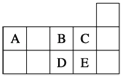
A. D�ڹ�����B��ȼ�յ���Ҫ����ΪDB3
B. C���⻯���ˮ��Һ���Ա�E��ǿ
C. D��B�γɵ������ӿ�����DB32����D2B42��
D. E�����������γ�����������Ժ�����Һ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com