
【题目】在容积可变的密闭容器中充入2 mol A和1 mol B发生反应:mA(g) + nB(g) ![]() pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
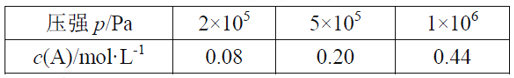
A. 维持压强2×105Pa,若反应开始后5min时达到平衡,则v(A)=0.016mol/(L·min)
B. P从2×105Pa增加到5×105Pa时,平衡逆向移动
C. P为1×106Pa时,平衡常数表达式K=![]()
D. 其它条件相同时,在上述三个压强下分别发生该反应。A的转化率随时间变化曲线如图所示
【答案】D
【解析】
由气体状态方程PV=nRT,得P=![]() RT即P=cRT,当温度相同时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,所以气体物质的计量数关系应为m+n=p。压强从5×105Pa增大到1×106Pa时,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol>0.4mol,浓度增大超过了2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面的分析,说明B在高压下变成液态或固体,由此分析解答。
RT即P=cRT,当温度相同时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,所以气体物质的计量数关系应为m+n=p。压强从5×105Pa增大到1×106Pa时,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol>0.4mol,浓度增大超过了2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面的分析,说明B在高压下变成液态或固体,由此分析解答。
A.题目中没有给出初始时容器体积,无法计算反应物A的初始浓度,也就无法计算在此条件下用A表示的反应速率,A项错误;
B.由气体状态方程PV=nRT,得P=![]() RT即P=cRT,当温度一定时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,B项错误;
RT即P=cRT,当温度一定时压强与气体的浓度成正比,由表格数据可知,压强从2×105Pa增大到5×105Pa,压强增大了2.5倍,此时A的浓度由0.08mol/L增大到0.20mol/L,恰好也增大了2.5倍,说明增大压强该平衡没有移动,B项错误;
C.由B项分析可知压强从2×105Pa增大到5×105Pa时平衡没有移动,说明反应前后气体分子数相等,即m+n=p。再从表格数据看,压强从5×105Pa增大到1×106Pa,压强增大了2倍,A的浓度由0.20mol/L增大到0.44mol,浓度增大的倍数大于2倍,说明此时平衡向逆反应方向移动了,根据勒夏特列原理,逆反应方向气体分子数应减小,结合前面分析可推断B在此压强下变成了液体或固体,所以压强为1×106Pa时B不是气体,其浓度视为常数,在平衡常数表达式中不应出现,即K=![]() ,C项错误;
,C项错误;
D.其它条件相同时,对于气体参加的反应增大压强反应速率增大,所以压强分别为1×106Pa、5×105Pa、2×105Pa下达到平衡(拐点)时所用时间依次增大。由B项分析知压强从2×105Pa增大到5×105Pa平衡没有移动,A的转化率相同。由C项分析知压强从5×105Pa增大到1×106Pa平衡向逆反应方向移动,A的转化率减小,图像与事实相符,D项正确;答案选D。


科目:高中化学 来源: 题型:
【题目】25 ℃时,把0.2 mol·L-1的醋酸加水稀释,则图中的纵轴y表示的是

A. 溶液中H+的物质的量
B. 溶液的导电能力
C. 溶液中的c(CH3COO-)/c(CH3COOH)
D. CH3COOH的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,1.7g氨气所占的体积为___L,它与标准状况下___L硫化氢含有相同数目的氢原子。
(2)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___g/mol,R的相对原子质量为____。
(3)已知CO、CO2的混合气体质量共16.0g,标准状况下体积为8.96L,则可推知该混合气体中含CO__g,所含CO 2 在标准状况下的体积为___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的分离与提纯是化学的重点,根据下列实验目的,分别选择相应的实验装置。

(1)除去氯化钠晶体中的碳酸钠______。
(2)除去碳酸钙中的氯化钠______。
(3)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合液(两者互溶):______。
(4)从溴水中提取溴______。
(5)除去氧化钙中的碳酸钙______。
(6)分离固体食盐和碘的方法______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
A.在空气中敞口久置的浓硫酸,溶液质量增大(脱水性)
B.浓硫酸可用来干燥某些气体(脱水性)
C.蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性)
D.在加热条件下铜与浓硫酸反应(氧化性、酸性)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积的关系如图,下列说法正确的是( )

①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A. ①④ B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向CH3COONa稀溶液中分别加入少量下列物质(忽略温度与体积变化),可以使![]() 的比值减小的是
的比值减小的是
A. KOH固体 B. 冰醋酸 C. CH3COONa固体 D. NaHSO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁酮酸乙酯( )和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示。
)和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示。

已知:①A是同系物中最小的直线形分子,且核磁共振氢谱显示其只有一种化学环境的氢;F为高聚物。
②![]() 不稳定会自动转化为RCH2CHO。
不稳定会自动转化为RCH2CHO。

回答下列问题:
(1)A中所含官能团是___________(填名称),B的结构简式为___________。
(2)E的名称为___________。
(3)写出反应⑥的化学方程式:____________________,该反应的反应类型为___________。
(4)由D制丁酮酸乙酯的反应产物中还有乙醇,制备过程中要加人适量的金属钠,其作用是______________________。(根据化学方程式和平衡移动原理回答)
(5)符合下列条件的丁酮酸乙酯的同分异构体有___________种。
a.能发生银镜反应 b.能与Na2CO3溶液反应放出气体
其中核磁共振氢谱显示为4组峰,且峰面积之比为1︰1︰2︰6的是___________(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有可逆反应2NO2(g) ![]() N2O4(g),△H<0,试根据下列图象判断t2、t3、t4时刻采取的措(只改变一种外部条件)。
N2O4(g),△H<0,试根据下列图象判断t2、t3、t4时刻采取的措(只改变一种外部条件)。
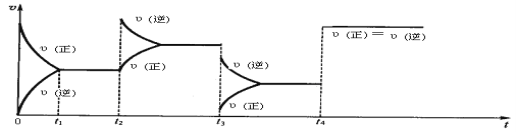
t2:___________________;t3:______________________ ;t4:______________________。
已知:A(g) + 2B(g) ![]() 2C(g) ΔH < 0。此反应的平衡常数表达式K=__________,温度降低,
2C(g) ΔH < 0。此反应的平衡常数表达式K=__________,温度降低,
K值会______(增大、减小、不变),A的转化率______________,化学反应速率________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com