
Ⅰ.某化学兴趣小组用以下装置探究SO2的某些化学性质。
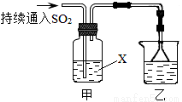
(1)装置乙的作用是 。
(2)若X为品红溶液,观察到溶液褪色,说明SO2具有 (填序号,下同);
若X为Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有 ;
a.氧化性 b.还原性 c.漂白性
(3)若试剂X为Ca(ClO)2溶液,可观察到白色沉淀生成,完成该过程的离子方程式:
 Ca2++
Ca2++ ClO-+
ClO-+ SO2+
SO2+ H2O=
H2O= CaSO4↓+
CaSO4↓+ Cl-+
Cl-+ SO42-+
SO42-+ 。
。
Ⅱ.某兴趣小组为探究沉淀溶解平衡的原理并测定某温度下PbI2溶度积常数,设计如下实验。
i.取100mL蒸馏水,加入过量的PbI2固体(黄色),搅拌,静置,过滤到洁净的烧杯中,得到滤液。
(4)搅拌的目的是 。
(5)取少量滤液于试管中,向其中滴加几滴0.1 mol·L-1KI溶液,观察到的现象是 。
ii.准确量取10.00mL滤液,与离子交换树脂(RH)发生反应:2RH + Pb2+= R2Pb + 2H+,交换完成后,流出溶液用滴定法测得n(H+)=3.000×10-5 mol。
(6)在此实验温度下,PbI2的溶度积常数Ksp= 。若步骤i盛装滤液的烧杯中有少量水,Ksp测定结果将会 (填“偏大”、“偏小”或“无影响”)。
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
下列化学反应,能用离子方程式H++OH- = H2O来表示的是( )
A.硫酸和NaOH溶液 B.醋酸和氢氧化钾溶液
C.盐酸和氢氧化镁 D.稀硝酸和氨水混合
查看答案和解析>>
科目:高中化学 来源:2017届广东省惠州市高三上第三次调研化学试卷(解析版) 题型:选择题
莽草酸是合成达菲的主要原料,其结构简式如图,下列说法正确的是:( )

A. 分子式为C7H8O5 B.能使溴的四氯化碳溶液褪色
C.只能发生加成反应和取代反应 D.分子中含有2种官能团
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省定西市通渭县高三上学期期末化学试卷(解析版) 题型:实验题
某校化学兴趣小组为研究Cl2单质的性质,设计如图所示装置进行实验.装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸.
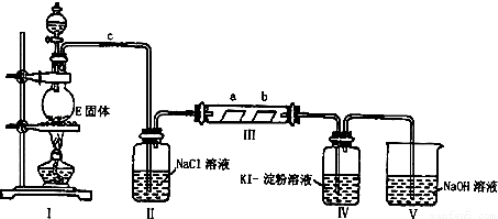
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是: ;
(2)加入药品前,检查Ⅰ中气体发生 装置气密性的操作是: ;
装置气密性的操作是: ;
(3)装置Ⅱ的作用是 ;
(4)实验过程中,装置Ⅳ中的实验现象为 ;发生反应的化学方程式为 ;
(5)实验结束后,该组同学在装置Ⅲ中观察b的红色退去,但是并未观察到“a无明显变化”这一预期现象,为了达到这一目的,你认为应在 之间还需添加洗气瓶(选填装置序号),该装置的作用是  ;
;
(6)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省定西市通渭县高三上学期期末化学试卷(解析版) 题型:选择题
化学与生活、社会发展息息相关,下列有关说法与氧化还原反应无关的是( )
A.KNO3、KClO3与单质S、C2H5OH不能混搭存放在同一库房间
B.缺铁性补血服用补铁剂时,需与维C同时服用
C.铜制品、铁制品 在潮湿的空气中生锈
在潮湿的空气中生锈
D.用乙醚从黄花蒿中提取青蒿素
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) + Y(g)  2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C.该温度下此反应的平衡常数K =1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上联考二化学卷(解析版) 题型:选择题
在强酸性无色溶液中,下列离子组能大量共存的是
A.Na+、K+ 、OH-、Cl- B.Na+、Cu2+、SO42-、NO3-
C.K+、Mg2+、SO42-、Cl- D.Ba2+、HCO32-、NO3-、K+
查看答案和解析>>
科目:高中化学 来源:2017届北京市海淀区高三上学期期末化学试卷(解析版) 题型:选择题
下列污水处理的方法中,表示其原理的离子方程式不正确的是
A.混凝法,用明矾做混凝剂:Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
B.中和法,用过量CO2中和碱性废水:CO2+2OH—=CO32—
C.沉淀法,用Na2S处理含Hg2+废水:Hg2++S2—=HgS↓
D.氧化还原法,用FeSO4将酸性废水中Cr2O72—还原为Cr3+:Cr2O72—+6Fe2++14H+=2Cr3++6Fe3++7H2O
查看答案和解析>>
科目:高中化学 来源:2017届广东省韶关市高三上高考调研理综化学试卷(解析版) 题型:填空题
高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
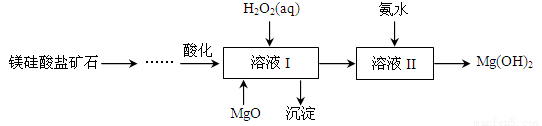
已知:①溶液I中除含Mg2+、SO42-外,还含少量Fe3+、Al3+、Fe2+等离子;
②Mg2+与氨水的反应为吸热反应。请回答下列问题:
(1)Mg在元素周期表中的位置为__________________。
(2)H2O2的电子式为________。溶液I中加入H2O2溶液发生反应的离子方程式是__________。
(3)向溶液I中首先加入的试剂是___________,产生沉淀的化学式为_________________。工业上有时只用一种含钠化合物替代H2O2和MgO,该试剂通常为___________(填化学式)。
(4)溶液II中Mg2+转化率随温度T的变化情况如图所示:
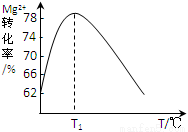
①向溶液II中加入氨水发生反应的离子方程式是______________________。
②T1前Mg2+转化率增大的原因是_________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com