
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70℃ | 57.6℃ |
| TiCl4 | -25℃ | 136.5℃ |
- 4 |
| ||
| 0.85cV |
| 10.00ml×pg/ml |
| 17cV |
| 200ρ |
| 17cV |
| 200ρ |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
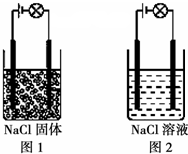 某化学兴趣小组按图示装置进行实验,观察到的实验现象为:图1灯泡不亮,图2灯泡亮,由此得出的结论正确的是 ( )
某化学兴趣小组按图示装置进行实验,观察到的实验现象为:图1灯泡不亮,图2灯泡亮,由此得出的结论正确的是 ( )| A、NaCl是非电解质 |
| B、NaCl溶液是电解质 |
| C、NaCl在水溶液中电离出了可以自由移动的离子 |
| D、NaCl溶液中水电离出大量的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ba2+、NO3-、SO42- |
| B、K+、Na+、CO32-、NO3- |
| C、K+、NH4+、MnO4-、Cl- |
| D、Mg2+、Al3+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
139 57 |
59 28 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
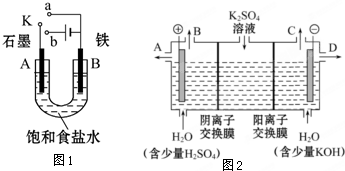 某课外活动小组用如图1装置进行实验,试回答下列问题.
某课外活动小组用如图1装置进行实验,试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com