
下图为10 mL一定物质的量浓度的HCl溶液用一定物质的量浓度的NaOH溶液滴定的图示。请根据图示计算:
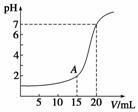
(1)氢氧化钠溶液物质的量浓度是多少?
(2)A点时溶液的pH是多少?
(1)0.05 mol·L-1 (2)2
解析 (1)根据题给图象可以看出,在氢氧化钠的体积为0时,盐酸溶液的pH=1,故可求出盐酸溶液的物质的量浓度为0.1 mol·L-1;再根据pH=7时,用去氢氧化钠溶液的体积为20 mL,此时盐酸与氢氧化钠恰好完全反应,则有0.01 L×0.1 mol·L-1=0.02 L×[NaOH],即[NaOH]=0.05 mol·L-1。
(2)A点时,显然盐酸是过量的,则加入的氢氧化钠与盐酸反应后剩余的盐酸为0.01 L×0.1 mol·L-1-0.015 L×0.05 mol·L-1=0.000 25 mol,此时,溶液的总体积为0.01 L+0.015 L=0.025 L,所以A点时溶液中的H+浓度为[H+]=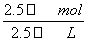 =1×10-2 mol·L-1,所以pH=2。
=1×10-2 mol·L-1,所以pH=2。


科目:高中化学 来源: 题型:
铁是人类较早使用的金属之一.运用铁及其化合物的知识,完成下列问题.
(1)所含铁元素既有氧化性又有还原性的物质是 (用字母代号填).
A.Fe; B.FeCl3; C.FeSO4; D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是 nm.
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: .某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05g.溶液中c(Cl﹣)= mol/L.
(4)若要验证该溶液中含有Fe2+,正确的实验方法是B.
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+;
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+;
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+.
(5)欲从废水中回收铜,并重新获得FeCl3溶液设计实验方案如下:
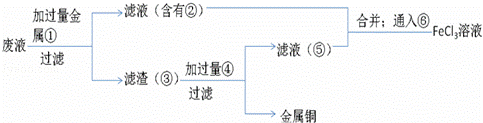
A.请写出上述实验中加入或生成的有关物质的化学式:
① ;② ;③ ;④HCl.
B.请写出通入⑥的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某容器中充入H2和N2,在一定条件下合成NH3,下列叙述不正确的是( )
A.开始反应时,正反应的速率最大
B.随着反应的进行,正反应的速率逐渐减小,最终减小为零
C.随着反应的进行,逆反应的速率逐渐增大,后保持不变
D.随着反应的进行,正反应的速率逐渐减小,最终与逆反应的速率相等且保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液一定显酸性的是( )
A.溶液中[OH-]>[H+]
B.滴加紫色石蕊试液后变红色的溶液
C.溶液中[H+]=10-6 mol·L-1
D.pH<7的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.HCl溶液中无OH-
B.NaOH溶液中无H+
C.KCl溶液中既无H+也无OH-
D.常温下,任何物质的水溶液中都有H+和OH-,且KW=1×10-14 mol2·L-2
查看答案和解析>>
科目:高中化学 来源: 题型:
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活动性由强到弱的顺序是( )
|
| A. | ①③②④ | B. | ①③④② | C. | ③④②① | D. | ③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH﹣ 2CO32﹣+6H2O,则下列说法错误的是( )
2CO32﹣+6H2O,则下列说法错误的是( )
|
| A. | 放电时CH3OH参与反应的电极为正极 |
|
| B. | 充电时电解质溶液的pH逐渐增大 |
|
| C. | 放电时负极的电极反应为:CH3OH﹣6e﹣+8OH﹣=CO32﹣+6H2O |
|
| D. | 充电时每生成1molCH3OH转移6mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)

回答下列问题:
(1)装置A中液体试剂选用 ,理由是 ____________________________。
(2)装置B的作用是 _________________________________________________,
装置E中碱石灰的作用是 ____________________________________________。
(3)装置D中发生反应的化学方程式是 ________,_________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com