
【题目】“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了高热值的煤炭气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛。生产煤炭气的反应之一是:
C(s)+H2O(g)![]() CO(g)+H2(g)ΔH=+131.4kJ/mol
CO(g)+H2(g)ΔH=+131.4kJ/mol
(1)在容积为3 L的密闭容器中发生上述反应,5 min后容器内气体的密度增大了0.12 g/L,用H2O表示0 ~ 5 min的平均反应速率为______________________。
(2)关于上述反应在化学平衡状态时的描述正确的是 。
A.CO的含量保持不变
B.v正(H2O)= v正(H2)
C.容器中混合气体的平均相对分子质量保持不变
(3)若上述反应在t0时刻达到平衡(如图),在t1时刻改变某一条件,请在右图中继续画出t1时刻之后正反应速率随时间的变化:
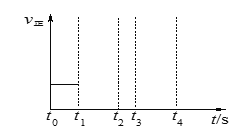
①缩小容器体积,t2时到达平衡(用实线表示);
②t3时平衡常数K值变大,t4到达平衡(用虚线表示)。
(4)在一定条件下用CO和H2可以制得甲醇,CH3OH和CO的燃烧热为别725.8 kJ/mol ,283.0 kJ/mol,水的摩尔蒸发焓为44.0 kJ/mol,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式: 。
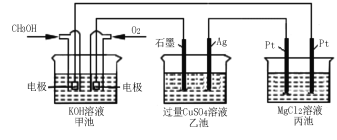
(5)如下图所示,以甲醇燃料电池作为电源实现下列电解过程。乙池中发生反应的离子方程式为 。当甲池中增重16 g时,丙池中理论上产生沉淀质量的最大值为 g。
【答案】(1)0.002mol∕L·min(2)ABC
(3)
(4)CH3OH(l)+O2(g)=CO(g)+2H2O(g)ΔH=-354.8kJ∕mol
(5)2Cu2++2H2O![]() 2Cu+O2+4H+;34.8
2Cu+O2+4H+;34.8
【解析】
试题分析:(1)5min后容器内气体的密度增大了0.12g/L,因此气体的质量增加了0.12g/L×3L=0.36g,根据方程式可知:

所以消耗水蒸气的物质的量浓度是0.03mol÷3L=0.01mol/L,因此用H2O表示0~5miin的平均反应速率为0.01mol/L÷5min=0.002mol/(L·min)。
(2)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A容器中CO的体积分数保持不变,说明反应得到平衡状态,A正确;正逆速率比等于系数比,v正(H2O)= v正(H2)一定平衡,B正确;c.生成物CO(g)和H2(g)的平均相对分子质量为15,反应前气体只有水,反应前后相对分子质量不同,容器中混合气体的平均相对分子质量保持不变一定平衡,C正确;(3)①缩小容器体积,体系中浓度变大,v正、v正突然变大,平衡逆向移动,v正再有变大的趋势,t2时到达平衡。②t3时平衡常数K值变大,说明改变条件是升高温度,v正、v正突然变大,平衡正向移动,v正再有变小的趋势,t4到达平衡;
(4)根据燃烧热的定义,为别725.8 kJ/mol ,283.0 kJ/mol,水的摩尔蒸发热为44.0 kJ/mol,则热化学方程式①CH3OH (l) +![]() O2 (g) =CO2 (g) + 2H2O (l) ΔH=-725.8 kJ ∕ mol ②CO (g) +
O2 (g) =CO2 (g) + 2H2O (l) ΔH=-725.8 kJ ∕ mol ②CO (g) +![]() O2 (g) =CO2 (g) ΔH=-283.0 kJ∕mol ③H2O (l)= H2O (g) ΔH=+44.0 kJ∕mol;根据盖斯定律①-②+③×2得CH3OH (l) + O2 (g) =CO (g) + 2H2O (g) ΔH=-354.8 kJ ∕ mol;(5)乙池为电解池,石墨是阳极,发生反应的离子方程式为2Cu2++2H2O
O2 (g) =CO2 (g) ΔH=-283.0 kJ∕mol ③H2O (l)= H2O (g) ΔH=+44.0 kJ∕mol;根据盖斯定律①-②+③×2得CH3OH (l) + O2 (g) =CO (g) + 2H2O (g) ΔH=-354.8 kJ ∕ mol;(5)乙池为电解池,石墨是阳极,发生反应的离子方程式为2Cu2++2H2O![]() 2Cu+O2+4H+;甲池中发生的反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O,溶液中甲醇和氧气反应后导致溶液质量增大,每反应2mol甲醇和3mol氧气反应溶液质量增加=2mol×32g/mol+3mol×32g/mol=160g,电子转移为12mol,当甲池中增重16g时,电子转移1.2mol,电子守恒得到丙池中理论上产生沉淀为氢氧化镁质量,MgCl2+2H2
2Cu+O2+4H+;甲池中发生的反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O,溶液中甲醇和氧气反应后导致溶液质量增大,每反应2mol甲醇和3mol氧气反应溶液质量增加=2mol×32g/mol+3mol×32g/mol=160g,电子转移为12mol,当甲池中增重16g时,电子转移1.2mol,电子守恒得到丙池中理论上产生沉淀为氢氧化镁质量,MgCl2+2H2![]() OMg(OH)2↓+H2↑+Cl2↑。电子转移1.2mol,生成氢氧化镁0.6mol,质量为0.6mol×58g/mol=34.8g
OMg(OH)2↓+H2↑+Cl2↑。电子转移1.2mol,生成氢氧化镁0.6mol,质量为0.6mol×58g/mol=34.8g


科目:高中化学 来源: 题型:
【题目】现有以下物质:①NaHCO3晶体②液态SO3③HF④盐酸⑤蔗糖⑥铜⑦KOH固体⑧氨水。请回答下列问题;
(1)属于非电解质的是________________,
(2)属于电解质的_______________,
(3)属于电解质的依次写出其在水中的电离方程式:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.肉桂酸甲酯由C、H、O三种元素组成,质谱分析其分子的相对分子质量为162,核磁共振氢谱谱图显示有6个峰,其面积之比为1:2:2:1:1:3,利用红外光谱仪检测其中的某些基团,测得红外光谱如下图:
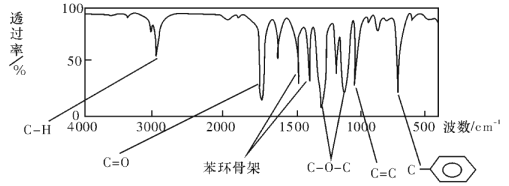
则肉桂酸甲酯的结构简式是 (不考虑立体异构)
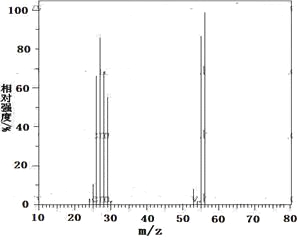
Ⅱ.现有2.8g有机物A,完全燃烧生成0.15molCO2和1.8gH2O,A的质谱图如下图所示:已知:![]() (X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
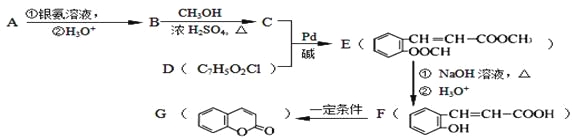
回答下列问题:
(1)A的分子式为 。
(2)写出C中含氧官能团名称: ;F→G 的反应类型是 。
(3)写出A和银氨溶液反应的化学方程式 。
(4)F有多种同分异构体,写出同时满足下列条件的两种同分异构体的结构简式: 。
Ⅰ.分子中除苯环外,无其它环状结构;
Ⅱ.苯环上有两个处于对位的取代基;
Ⅲ.能发生水解反应,不能与Na反应;
Ⅳ.能与新制Cu(OH)2按物质的量比1:2发生氧化反应
(5)又知:![]() (R,R′为烃基),试写出以苯和丙烯(
(R,R′为烃基),试写出以苯和丙烯(![]() =CH—CH3)为原料,合成
=CH—CH3)为原料,合成![]() 的路线流程图: 。
的路线流程图: 。
合成路线的书写格式如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关H2SO4的叙述正确的是( )
A.H2SO4的相对分子质量是98g/mol
B.1molH2SO4的质量是98g
C.1molH2SO4中含有1molH2
D.1molH2SO4中共含有6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的温度和压强下,相同体积的任何气体都含有相同数目的粒子。同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
A.物质的量之比为16∶11 B.密度之比为11∶16
C.摩尔质量之比为11∶16 D.体积之比为11∶16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积不变的400℃恒温密闭容器中,一定量的SO2与1mol O2在催化剂作用下发生反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH =-Q kJ ∕ mol(Q﹥0)。当气体的物质的量减少0.5 mol时反应达到平衡。下列叙述错误的是( )
2SO3(g) ΔH =-Q kJ ∕ mol(Q﹥0)。当气体的物质的量减少0.5 mol时反应达到平衡。下列叙述错误的是( )
A.增大氧气浓度,平衡正向移动,平衡常数不变
B.降低温度,正反应速率比逆反应速率减小的程度小
C.平衡时SO2气体的转化率为50%
D.该条件下反应放出0.5Q kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,有下列气体分子数相同的可逆反应,其平衡常数K值分别如下:
①H2+F2=2HF K=1047 ②H2+Cl2=2HCl K=1017
③H2+Br2=2HBr K=109 ④H2+I2=2HI K=1
试判断平衡时各反应的正反应进行的程度由大到小的顺序是
A. ①②③④ B. ④②③① C. ①④③② D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化工生产原理错误的是:①可以用电解熔融的氯化铝的方法来制取金属铝 ②可以把钠加入氯化镁饱和溶液中制取镁 ③用热分解法冶炼铁 ④湿法炼铜是用锌和硫酸铜溶液反应置换出铜
A.②③ B.①③ C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 向BaCl2溶液中加入适量Na2CO3溶液后,静置,向上层清液中继续滴加Na2CO3溶液,若无沉淀,说明Ba2+已经完全沉淀
B. 淀粉在稀硫酸的作用下水解后,加NaOH溶液使溶液呈碱性,加入新制Cu(OH)2,加热,若有红色沉淀生成,说明淀粉已经完全水解
C. 将Na2SO4·10H2O晶体置于坩埚中加热,冷却后称量,并重复上述操作,若相邻两次称量的结果相同,说明硫酸钠已全部失去结晶水
D. 用酸式滴定管向滴有酚酞的NaOH溶液中滴加标准HCl溶液,若滴入最后一滴HCl溶液后粉红色刚好褪去,说明已达滴定终点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com