
【题目】一定条件下,可逆反应X(s)+Y(g)![]() W(g)+Z(g)(正反应是放热反应),在一定体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如图所示。下列条件的改变与图中情况相符的是( )
W(g)+Z(g)(正反应是放热反应),在一定体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如图所示。下列条件的改变与图中情况相符的是( )
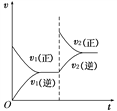
A. 增加了X的物质的量 B. 降低了温度
C. 增大了压强 D. 增大了Y的物质的量
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】碘水溶液中存在下列平衡:I2(aq)+I-(aq)=I3-(aq)。测得不同温度下该反应的平衡常数K如表所示,下列说法正确的是
t/℃ | 5 | 15 | 25 | 35 | 50 |
K | 1100 | 841 | 689 | 533 | 409 |
A. 反应I2(aq)+I-(aq)![]() I3-(aq)的ΔH>0
I3-(aq)的ΔH>0
B. 25℃时,向溶液中加入少量KI固体,平衡常数K小于689
C. 其他条件不变,升高温度,溶液中c( I3-)减小
D. 该反应的平衡常数表达式为K=c(I-)/c(I3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下表:
温度/℃ | 200 | 300 | 400 | 500 | 600 |
氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是_______。
(2)在一定温度下,将2molN2和6molH2通入到体积为2L的密闭容器中,发生反应N2+3H2![]() 2NH3,2min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=_______________(结果用最简分数表示);欲使K增大,可以采取的措施是______。
2NH3,2min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=_______________(结果用最简分数表示);欲使K增大,可以采取的措施是______。
(3)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是______(选填序号字母)
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂
(4)NH3能分解为N2和H2,在相同条件下,测得分解后混合气体密度为分解前的2/3,则氨的分解率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是__________________________。
(2)利用实验1中的数据,计算用KMnO4表示的化学反应速率为_____________。(溶液混合前后体积变化可忽略)
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
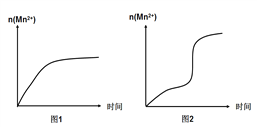
①该小组同学提出的假设是_____________。
②请你帮助该小组同学完成实验方案,并填写表中空白
实验编号 | 室温下,试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | |||
4 | _____________ | 2.0 | 2.0 | 3.0 | MnSO4 | t |
③若该小组同学提出的假设成立,t_____________1.5(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一小块钠投入盛有煤油(与水不相溶)和水的烧杯中,可以观察到的现象是
A. 钠浮在烧杯中的液面上 B. 钠沉在烧杯的底部
C. 钠会在水和煤油的交界面上下浮动,直到反应结束 D. 煤油会燃烧起来,产生很浓的黑烟
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A. 1 mol FeI2与足量氯气反应时转移的电子数为2NA
B. 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
C. 18gD2O和18gH2O中含有的质子数均为10NA
D. 1 mol Na2CO3固体中含离子总数小于3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,1体积水溶解700体积氨气,所得溶液密度为0.9gcm﹣3 , 这种氨水的物质的量浓度和溶质的质量分数分别为( )
A.18.4molL﹣1 34.7%
B.20.4molL﹣1 38.5%
C.18.4molL﹣1 38.5%
D.20.4molL﹣1 34.7%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下二氯化二硫(S2 Cl2)为红棕色液体,其结构式为Cl-S-S-Cl。其制备反应及与水反应的化学方程式如下:①CS2+3Cl2![]() CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2↑+3S↓,则下列说法正确的是
CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2↑+3S↓,则下列说法正确的是
A. 反应①中CS2作氧化剂
B. 反应①中每生成1mol S2Cl2转移4mol电子
C. 反应②中氧化产物与还原产物的物质的量之比为3:1
D. 反应②中S2Cl2既作氧化剂又作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com