
| A. | 将适量的发酵粉放在容器中加热,观察气体的产生 | |
| B. | 在洁净的水杯中先加入小苏打粉,再加入食醋,观察气体 | |
| C. | 往稀白粥中加入少量加碘食盐,检验加碘食盐中含有I2 | |
| D. | 在一瓣橘子上插入两根铜丝并与小灯泡连接,验证电流的产生 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
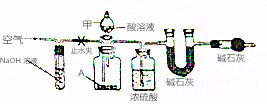 碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋 | B. | 白酒 | C. | 食盐 | D. | 葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的醋酸的导电能力比纯醋酸的导电能力弱 | |
| B. | PH均为5的盐酸和NH4Cl溶液中水电离出来的c(H+)均为1×10-5mol•L-1 | |
| C. | PH=8.3的NaHC03溶液中:c(Na+)>c(HCO3- )>c(CO32-)>c(H2CO3) | |
| D. | 向0.10mol•L-1 NaHSO3溶液中通入NH3至溶液的PH=7,此时溶液中:c(Na+)>c(SO32-)>c(NH4+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com