
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。

(1)B装置的作用是________________________________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中定有______气体产生,写出D中发生反应的离子方程式____________________。若去掉C,是否能得出同样结论并解释其原因__________________________。
(3)A中固体分解后产生NH3,写出其两种用途________________________________________。
(4)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3而不含FeO。请完成表内容。(试剂,仪器自选)
实验步骤 | 预期现象 | 结论 |
①取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解; ②______________________________________________________ | 固体残留物仅为Fe2O3 |
(5) 用实验的方法验证C溶液含有NH4+___________________________________________。
【答案】 检验产物中是否有水生成 SO2 SO2+H2O2+Ba2+=BaSO4↓+2H+ 否,若有,SO3也有白色沉淀生成 作制冷剂、做氮肥 将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液;若高锰酸钾溶液不褪色,加入KSCN溶液后变红 取少量样品于洁净的试管中,加入浓NaOH并加热,产生的气体若能使湿润的红色石蕊试纸变蓝,说明C溶液含有NH4+反之,则无。
【解析】(1)B装置中无水硫酸铜遇到水变蓝色,所以装置B的作用是检验产物中是否有水生成;
(2)实验中,观察到C中盐酸酸化的氯化钡溶液中无明显现象,证明无SO3生成,D中过氧化氢具有氧化性,能氧化SO2生成硫酸,结合钡离子生成硫酸钡白色沉淀,可确定产物中一定有SO2;装置D中反应的离子方程式为SO2+H2O2+Ba2+=BaSO4↓+2H+;若去掉C,生成的SO3进入装置D中也能生成白色沉淀,所以不能得出同样的结论;
(3)NH3的用途很多,主要的有可用于制硝酸、制氮肥、作制冷剂等;
(4)A中固体完全分解后变为红棕色粉末,要验证该粉末仅为Fe2O3,而不含FeO,先加稀硫酸使其完全溶解后,将溶液分成两份,分别滴加高锰酸钾溶液和KSCN溶液,预期的反应现象为:若高锰酸钾溶液不褪色,证明不含FeO,加入KSCN溶液后变红,说明有Fe2O3生成;
(5)装置C中是盐酸酸化的氯化钡溶液呈酸性,能够吸收NH3生成NH4+,检验NH4+的方法是:取少量样品于洁净的试管中,加入NaOH浓溶液并加热,若产生的气体能使湿润的红色石蕊试纸变蓝,说明C溶液含有NH4+,否则,则不含NH4+。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
2SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是

A. 该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数
B. 500℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-2a kJ·mol-l
2SO3(g) ΔH=-2a kJ·mol-l
C. 该反应中,反应物的总键能小于生成物的总键能
D. ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用双线桥法表示反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O化合价的升降和电子的转移情况,并回答下列问题:
标双线桥:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O_______。
该反应的氧化产物是________。若有1mol KMnO4参加反应,转移的电子的物质的量是_____,被氧化的HCl的物质的量是________。
(2)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中制得:SiO2+C+N2![]() Si3N4+CO。
Si3N4+CO。
①配平上述反应的化学方程式(将化学计量数填在答题卡相应的横线上)____;
②该反应的氧化剂是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A的结构简式如下:
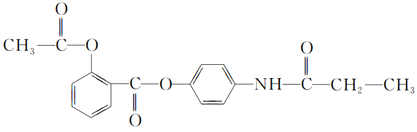
(1)A的分子式是________。
(2)A在NaOH水溶液中充分加热后,再加入过量的盐酸酸化后,可得到B、C、D和![]() 四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
(3)下列物质中,不能与B发生化学反应的是________(填空序号)。
①浓H2SO4和浓HNO3的混合液 ②CH3CH2OH(酸催化) ③CH3CH2CH2CH3 ④Na ⑤浓溴水
(4)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式为_________________。
(5)写出B与碳酸氢钠反应的化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的是细胞中含有的四种有机物的结构与功能。请据图回答下列问题。

(1)图中E含有的元素有_____,A是_____,A形成E的方式为_____。
(2)图中的F为_____。
(3)图中G在植物体内主要是_____,在动物体内主要是_____。
(4)图中H是_____,每克该物质完全氧化分解放出的能量约为39 kJ。
(5)仅由E、F两种物质构成的生物是_____。
(6)E在细胞内的合成受F、G、H中的_____控制。
(7)由C构成的植物细胞特有的结构物质是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质互为同系物的一组是( )
A.35Cl和37ClB.CH3CH2OH和CH3OCH3
C.CH3COOH和HCOOHD.CH4和C2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种香豆素衍生物,可以用作香料,其合成路线如下:
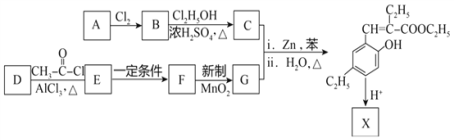
已知: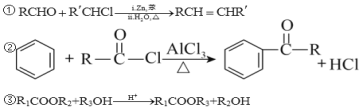
(1)A所含官能团的名称是___________。
(2)B生成C反应的化学方程式是___________________________________________。
(3)G的结构简式是____________________。
(4)F的结构简式是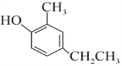 。D的分子式是C7H8O,与F互为同系物。D的结构简式是________。
。D的分子式是C7H8O,与F互为同系物。D的结构简式是________。
(5)X的分子式是C13H14O2,X与足量NaOH溶液共热的化学方程式是________________。
(6)E可以经多步反应合成F,请写出一条可能的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】秦皮是一种常用的中药,具有抗炎镇痛、抗肿瘤等作用。“秦皮素”是其含有的一种有效成分,结构简式如下图所示,有关其性质叙述不正确的是

A. 1mol该有机物能与5mol H2反应
B. 该有机物分子式为C10H8O5
C. 该有机物能发生加成;氧化,取代等反应
D. 分子中有四种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A. 在常温常压下,11.2 L O2含有的分子数为0.5NA
B. 71 g Cl2所含原子数为2NA
C. 标准状况下,22.4 L H2O含有的分子数为NA
D. 25℃、101Kpa时,64g SO2中含有的分子数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com