
| A. | 氯化钠晶体熔化 | B. | 电解水 | ||
| C. | 碘升华 | D. | 硫化氢受热分解为氢气和硫 |
分析 先判断断键方式,再判断克服的作用力,只需克服分子间作用力,则晶体为分子晶体,且未发生化学键断裂.
A.氯化钠属于离子晶体,氯化钠晶体熔化破坏化学键;
B.水属于分子晶体,电解水发生化学变化;
C.碘单质属于分子晶体,碘升华属于物质的状态变化;
D.硫化氢属于分子晶体,硫化氢受热分解为氢气和硫发生化学反应.
解答 解:A.氯化钠晶体是离子晶体,微粒间的作用力是离子键,氯化钠晶体熔化离子键被破坏,故A错误;
B.电解水生成氢气、氧气,发生化学变化,破坏是氢、氧间的共价键,故B错误;
C.固体碘升华,只破坏分子间作用力,故C正确;
D.硫化氢属于分子晶体,硫化氢受热分解为氢气和硫,破坏是氢、硫间的共价键,故D错误;
故选C.
点评 本题考查物质的成键方式,此类题的解题方法是:先判断断键方式,再判断克服的作用力,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | Cu3+ | Ni3+ | Fe3+ | Al3+ | Cr3+ |
| 浓度(mg/L) | 7000 | 7000 | 2500 | 4200 | 3500 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 70% | C. | 47.6% | D. | 52.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
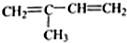 ⑤
⑤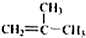
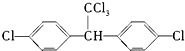
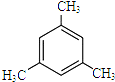 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
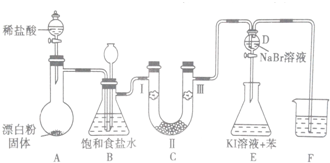
| 编号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | C | C. | S | D. | Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子带电荷并且在一定条件下能稳定存在 | |
| B. | 胶体的分散质粒子直径在1nm~100nm之间 | |
| C. | 胶体粒子不能穿过半透膜,能通过滤纸空隙 | |
| D. | 胶体粒子能够发生布朗运动而且能产生丁达尔现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com