
【题目】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:
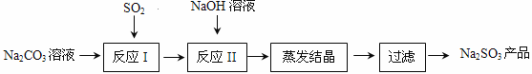
(1)SO2对环境的危害主要是形成 。
(2)用Na2CO3溶液能吸收SO2的原因是 。
(3)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中发生如下反应:
①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
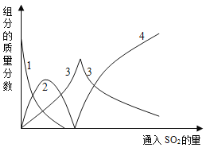
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为 (填化学式)。
(4)实验时,“反应II”中加入NaOH溶液的目的是 (用化学方程式表示)。
(5)获得的Na2SO3产品久置后质量变重,主要原因是 。
【答案】(1)酸雨
(2)亚硫酸的酸性比碳酸强(或Na2CO3溶液呈碱性)
(3)NaHCO3
(4)NaHSO3+NaOH=Na2SO3+H2O
(5)Na2SO3易被氧化成Na2SO4
【解析】
试题分析:(1)二氧化硫可以形成酸雨;(2)二氧化硫溶于水后生成亚硫酸,亚硫酸的酸性比碳酸强所以二氧化硫能与碳酸钠反应生成二氧化碳;(3)线2表示的物质先增加,后减小,当其消失时会出现另一种物质,结合方程式分析,只有碳酸氢钠符合题意,反应先生成碳酸氢钠,后碳酸氢钠与二氧化硫反应逐渐减少,当碳酸氢钠完全反应后才产生亚硫酸氢钠,故答案为:NaHCO3;(4)加入氢氧化钠是为了和亚硫酸氢钠反应生成亚硫酸钠,反应的方程式为:NaHSO3+NaOH=Na2SO3+H2O;(5)Na2SO3易被氧化成Na2SO4,物质的质量增加。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】下列有关230Th和232Th的说法正确的是
A.230Th和232Th的核外电子数不同
B.230Th和232Th的化学性质不同
C.230Th和232Th互为同位素
D.230Th和232Th是同一种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组设计出利用工业废酸(含10%的H2SO4)和废弃氧化铜锌矿制取活性ZnO的方案如图。
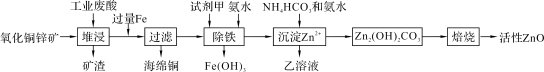
已知:298 K时各离子开始沉淀及完全沉淀时的pH如下表所示。
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 6.34 | 9.7 |
Fe3+ | 1.48 | 3.2 |
Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)____Ksp(ZnS)(选填“>”、“<”或“=”)。
(2)除铁过程中试剂甲最好选用____(填序号)。
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在____范围之间。
(4)试写出沉淀Zn2+时发生反应的离子方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用过量的碳还原二氧化硅制得粗硅,同时得到一种可燃性气体;
② 粗硅与干燥的HCl气体反应制得SiCl3(Si+ 3HCl![]() SiCl3 + H2)
SiCl3 + H2)
③ SiHC13与过量的H2在1100~1200℃的温度下反应制得纯硅,已知SiHCi3。能与水剧烈反应,在空气中易自燃。
请回答:
(1)第一步制取粗硅的化学反应方程式为_________。
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃ )中含有少量SiC14 (沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHC13采用的方法为________。
(3)实验室用SiHCl3 与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是___________,装置C中的烧杯需要加热,目的是___________。
②反应一段时间后,装置D中观察到的现象是___________,装置D不能采用普通玻璃管的原因是___________,装置D中发生反应的化学方程式是___________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四种化合物①NaHCO3、②Al(OH)3、③Al2O3、④NaAlO2中,与盐酸和氢氧化钠溶液都能反应的是( )
A.只有②④ B.只有①② C.只有①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室模拟工业生产碳酸钠:一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2,一段时间后,出现沉淀,过滤得到NaHCO3晶体。
(1)该过程的化学方程式: 。
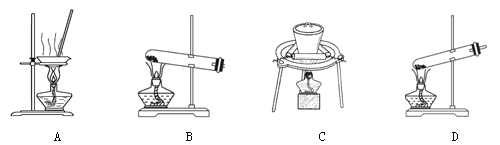
(2)加热NaHCO3得到纯碱制品,实验室可进行此操作的装置是 。
(3)得到的纯碱制品含有少量NaHCO3和NaCl,设计实验验证样品中各种组分。
试剂和仪器限选用:试管、胶头滴管、过滤装置、Ba(NO3)2溶液、NaOH溶液、AgNO3溶液、澄清石灰水、稀硫酸、稀盐酸、稀硝酸。
步骤一:取少量制品于试管中,加少量蒸馏水,振荡,溶解。往试管中加入 振荡,观察; | 现象:溶液中产生大量白色沉淀; 结论: 。 |
步骤二:将步骤一的浊液过滤,取滤液于试管中B中,加入 , 振荡,观察; | 现象: ; 结论:样品中含有NaHCO3。 |
步骤三:将步骤二的浊液过滤,取滤液于试管C中, 振荡,观察。 | 现象: ; 结论: 。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ有机物A、B、C、D、E之间发生如下的转化:

(1)写出C物质的结构简式:_________________。
(2)上述②~⑧转化反应中,属于取代反应的有____________;
(3)属于加成反应的有____。(用反应序号填写)
(4)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是______________。
请写出下列转化的化学反应方程式:
(5)B+D~E:________________________;
(6)乙烯生成聚乙烯:___________________。
Ⅱ己知葡萄糖在乳酸菌的作用下转化为乳酸,乳酸的结构简式为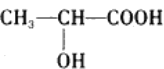 。
。
试回答:
(7)乳酸分子中含有_____和_______两种官能团(写名称)。
(8)乳酸与金属钠反应的化学方程式为________________。
(9)乳酸与Na2CO3溶液反应的化学方程式为___________________________。
(10)乳酸在浓硫酸作用下,两分子相互发生酯化反应生成环状酯,此环状酯的结构简式为 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求填空
(1)甲基的电子式 电石气的结构式 ___________________
(2)写出下列有机物的系统命名:CH3CH(C2H5)CH(CH3)2______
(3)写出下列各种有机物的结构简式.
①2,3﹣二甲基﹣4﹣乙基已烷 .
②支链只有一个乙基且式量最小的烷烃 .
(4)充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是相同条件下N2的2倍.
①求该有机物的分子式 .
②该有机物链状同分异构体的结构简式为: 、 、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ca2+、Ba2+、
CO32-、SO42-,现取三份100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,
沉淀质量为4.66g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl- (是或否)
(2)由第二份进行的实验可知混合物中应含 离子,其物质的量浓度为 。
(3)由第三份进行的实验可知12.54g 沉淀的成份为 。请计算形成该沉淀的原混合物中各离子的物质的量 。
(4)综合上述实验,你认为以下结论正确的是( )
A.该混合物中一定含有K+、NH4+、CO32-、SO42-,可能含有Cl-,且n(K+)≥0.04mol
B.该混合物中一定含有NH4+、CO32-、SO42-,可能含有Ca2+、 K+、Cl-
C.该混合物中一定含有NH4+、CO32-、SO42-,可能含有K+、Cl-
D.该混合物中一定含有NH4+、SO42-,可能含有Ca2+、K+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com