
| A. | 100g质量分数为46%的酒精水溶液中的氧原子数为4NA | |
| B. | 500mL 2mol/L碳酸钠溶液中的阴离子数小于NA | |
| C. | 合成氨反应中催化剂降低了反应的活化能,增大了反应的焓变 | |
| D. | 据“△H-T•△S<0”判断某反应能自发,可知该反应一定能发生 |
分析 A.水溶液中水中也含氧原子;
B.碳酸根离子水解生成碳酸氢根离子和氢氧根离子;
C.焓变等于生成物能量和与反应物能量和的差,对于一个反应,在相同的温度压强下焓变是定值;
D.△G=△H-T•△S<0时,只能说明反应能自发进行,不能说明此反应一定能发生.
解答 解:A.溶剂水中含有氧原子,100g46%酒精水溶液含氧原子总数大于4NA,故A正确;
B.500mL 2mol/L碳酸钠相当于1mol碳酸钠,碳酸钠在水中发生水解,当生成碳酸氢钠时,每有1mol碳酸氢钠生成同时生成1mol氢氧根,所以溶液中阴离子大于NA,故B错误;
C.焓变等于生成物能量和与反应物能量和的差,对于一个反应,在相同的温度压强下焓变是定值,故焓变不变,故C错误;
D.△G=△H-T•△S<0时,只能说明反应能自发进行,不能说明此反应一定能发生,故D错误,
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 5倍 | B. | 4倍 | C. | 3 倍 | D. | 2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水淡化的方法有蒸馏法、离子交换法、电渗析法等 | |
| B. | 明矾水解时能生成具有吸附性的胶体粒子,故可用于消毒杀菌 | |
| C. | Ba2+对人体无毒,故BaSO4在医学上可用作“钡餐” | |
| D. | 与铜质水龙头连接处的铜质水管不易发生腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12的有机物有三种,它们互为同系物 | |
| B. | C4H8C12有9种同分异构体(不考虑立体异构) | |
| C. | 石蜡油、苯、四氟乙烯都不能使溴水褪色 | |
| D. | 等物质的量的甲烷与氯气反应后体积保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
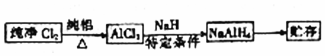
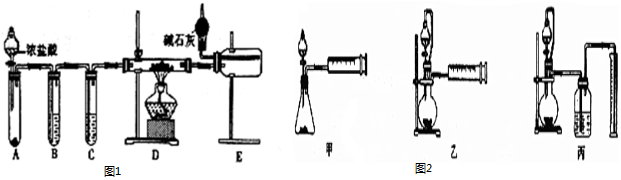
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
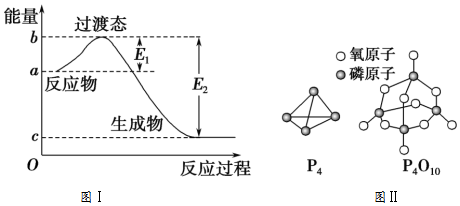
| 化学键 | P-P | P-O | O═O | P═O |
| 键能/(kJ/mol) | a | b | c | x |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
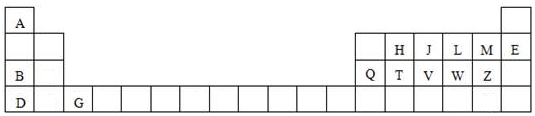
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 目的 | 古代文献 | 说明 | |
| A | 使用 | 《周礼》:“煤饼烧蛎房(牡蛎壳)成灰”,蔡伦造纸用此“灰”溶于水沤浸树皮脱胶. | “灰”的主要成分是氧化钙 |
| B | 鉴别 | 《新修本草》:硝石“如握盐雪不冰,强烧之,紫青烟起”,用于区分硝石(KNO3)和朴硝(Na2SO4) | 利用颜色反应 |
| C | 浸出 | 《肘后备急方》:“青蒿一握,以水二升渍,绞取汁,尽服之”. | 提取青蒿素中的纤维素 |
| D | 性质 | 《本草纲目》:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧机诸药者”. | 利用KNO3的氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com