
 ijdz��ɫ����X[x��NH4��2SO4•yFeSO4•zH2O]�ڷ�����ѧ�ϳ�������ԭ����Ϊȷ������ɣ�ijС��ͬѧ��������ʵ�飮
ijdz��ɫ����X[x��NH4��2SO4•yFeSO4•zH2O]�ڷ�����ѧ�ϳ�������ԭ����Ϊȷ������ɣ�ijС��ͬѧ��������ʵ�飮���� I����1��������Һ����ʽ�ζ�����ȡ��
��2������������ˮ�����ȿ���ʹ������ȫ�ݳ���
��3���ζ�ǰ�ζ��ܼ��������ݣ��ζ���������ʧ�������ĵ�NaOH����Һ�����ƫ�������NaOH��Ӧ����������ʵ���ƫ�����백����Ӧ����������ʵ���ƫС��
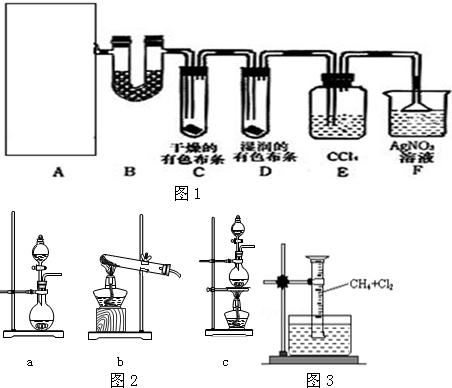
II����4���ж��Ȼ����Ƿ�������������ϲ���Һ�м����μ��Ȼ������۲�����
��5������ˮϴ�ӿ��Լ��ٹ�����ܽ⣻
��6���������յ�ʵ�����������
��7�����ݵζ�ʱ���ĵ��������Ƶ����ʵ�����������백����Ӧ����������ʵ������Լ����������ʵ������������ᱵ�����������������������ʵ�������Ͼ�������������ѧʽ��x��y��z��ֵ�����ɵó�����X�Ļ�ѧʽ��
��� �⣺I����1��������Һ����ʽ�ζ�����ȡ������ȷ��ȡ����Ӧ��ѡ����ʽ�ζ��ܣ��ʴ�Ϊ����ʽ�ζ��ܣ�
��2������X��NaOH��Ӧ���ɰ���������������ˮ�����ȿ���ʹ������ȫ�ݳ�����������Һ��ȫ���գ��ʴ�Ϊ�������ɵ�NH3ȫ����������������Һ��ȫ���գ�
��3���ζ�ǰ�ζ��ܼ��������ݣ��ζ���������ʧ�������ĵ�NaOH����Һ�����ƫ�������NaOH��Ӧ����������ʵ���ƫ�����백����Ӧ����������ʵ���ƫС�����Լ���õ��İ��������ʵ���ƫС���ʴ�Ϊ��ƫС��
II����4���ж��Ȼ����Ƿ�������������ϲ���Һ�м����μ��Ȼ�������û���µij���������˵����Һ��û����������ӣ����Ȼ����Ѿ�������
�ʴ�Ϊ������Һ�ֲ�����ϲ���Һ�м���1��2��BaCl2��Һ���ް�ɫ���dz��֣���BaCl2��Һ�ѹ�����
��5������ˮϴ�ӿ��Լ��ٹ�����ܽ⣬������ϴ�ӻ�ʹ�����ϸ�����������ӣ���Һ��Ҳ������������ӣ����Բ������������Һϴ�ӳ�����Ӧ��ѡ����ˮϴ�ӣ�
�ʴ�Ϊ��A��
��6�������յ�ʵ��ʱ�����������������գ��þƾ��Ƽ��ȣ������������������ǵ����ż��ϣ������õ�������Ϊ�����������żܡ������ǡ��ƾ��ƣ�
�ʴ�Ϊ��BDF��
��7����NaOH��Ӧ����������ʵ���Ϊn��H2SO4��=$\frac{1}{2}$n��NaOH��=$\frac{1}{2}$��0.0400mol•L-1��0.02500L��
�백����Ӧ����������ʵ���Ϊ��0.05L��1.0100mol•L-1-$\frac{1}{2}$��0.0400mol•L-1��0.025L=0.05mol�����������ʵ���n��NH3��=2n��H2SO4��=0.1mol��
19.60g����X���ձ��У���ˮ�ܽ⣬�߽����������� BaCl2��Һ���õ����ᱵ����23.30g����n��SO42-��=$\frac{23.30g}{233g/mol}$=0.10mol��
$\frac{19.60g}{132x+152y+18z}$��2x=0.1mol��$\frac{19.60g}{132x+152y+18z}$����x+y��=0.1mol����x+y=2x����x=y��
��x=1����$\frac{19.60}{132+152+18z}$��2=0.1����z=6����x=1��y=1��z=6�����仯ѧʽΪ��NH4��2SO4•FeSO4•6H2O��
��x=2����$\frac{19.60}{132��2+152��2+18z}$��4=0.1����z=1.21�������ϣ�
�ʴ�Ϊ����NH4��2SO4•FeSO4•6H2O��
���� ���⿼��������ɵ�̽��ʵ�飬���շ����Ļ�ѧ��Ӧ��ʵ�����Ϊ���Ĺؼ������ط������������������Ŀ��飬ע����Ϣ����ѧ֪ʶ�Ľ�ϣ���Ŀ�Ѷ��еȣ�


 ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д� �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�дﵽƽ��ʱ������O2������������NO������֮�Ȳ�Ϊ5��4 | |
| B�� | ����λʱ������xmolNO��ͬʱ������xmolNH3����Ӧ�ﵽƽ��״̬ | |
| C�� | �ﵽƽ��״̬��NH3��O2��NO��H2O��g�������ʵ������ֲ��� | |
| D�� | �ﵽƽ��״̬ʱ�������������������Ӧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�28gCH2=CH2����NA��̼ԭ�� | |
| B�� | 1mol������3NA��̼̼������3NA��̼̼˫�� | |
| C�� | ��״���£�22.4L�����麬��12NA����ԭ�� | |
| D�� | ���³�ѹ�£�16gCH4����4NA�����ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȫ�� | B�� | �٢ڢ� | C�� | �٢� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| W | X | |
| Y | Z |
| A�� | ZԪ�ص��������Ӧˮ���������һ��ǿ��Y | |
| B�� | X��Y��Z������⻯���ȶ�����������Y | |
| C�� | XԪ�صļ����ӻ�ԭ�Դ���Y | |
| D�� | ZԪ�ص����ڻ�ѧ��Ӧ��ֻ���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com