
【题目】下列溶液中Cl-的物质的量浓度和Cl-的物质的量与50mL1mol/L的AlCl3溶液中Cl-物质的量浓度和Cl-的物质的量都相等的是
A. 75mL3mol/L的NH4Cl B. 150mL1mol/L的NaCl
C. 50mL1.5mol/L的CaCl2 D. 50mL3mol/L的NaClO
【答案】C
【解析】
50mL1mol/L的AlCl3溶液中Cl-物质的量浓度:c(Cl-)=1mol/L×3=3mol/L,Cl-的物质的量是n(Cl-)=3mol/L×0.05L=0.15mol。根据Cl-的物质的量浓度等于电解质浓度与化学式中含有Cl-数目的乘积,利用c=![]() ,计算溶液中Cl-离子的物质的量。
,计算溶液中Cl-离子的物质的量。
50mL1mol/L的AlCl3溶液中Cl-物质的量浓度:c(Cl-)=1mol/L×3=3mol/L,n(Cl-)=3mol/L×0.05L=0.15mol。
A.75 mL3 mol/L的NH4Cl溶液中:c(Cl-)=3mol/L×1=3mol/L,n(Cl-)=3mol/L×0.075L=0.225mol,与50mL1mol/L的AlCl3溶液中Cl-物质的量不等,A错误;
B.150 mL1 mol/L的NaCl溶液中:c(Cl-)=1mol/L×1=1mol/L,氯离子的浓度与50mL1mol/L的AlCl3溶液中Cl-物质的量浓度不相等,B错误;
C.50 mL1.5 mol/L的CaCl2溶液中:c(Cl-)=1.5mol/L×2=3mol/L,Cl-的物质的量为:n(Cl-)=3mol/L×0.05L=0.15mol,符合条件,C正确;
D.50 mL 3 mol/L的KClO3溶液中不存在氯离子,D错误;
故合理选项是C。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】利用右图装置进行实验,甲乙两池均为1 mol·L–1的AgNO3溶液,A、B均为Ag电极。实验开始先闭合K1,断开K2。一段时间后,断开K1,闭合K2,形成浓差电池,灵敏电流计指针发生偏转(提示:Ag+ 浓度越大,氧化性越强),下列说法不正确的是
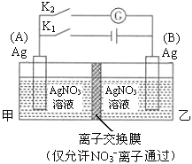
A.闭合K1,断开K2后,A电极增重
B.闭合K1,断开K2后,乙池溶液中Ag+浓度增大
C.断开K1,闭合K2后,B电极发生氧化反应
D.断开K1,闭合K2后,NO3–向A电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向80mL浓硫酸中加入56g铜片,加热一段时间后,至不再反应为止,计算:
(1)实验测得反应中共有13.44L标准状况下的SO2生成,被还原的硫酸的物质的量为_____mol,反应中转移的电子有_____mol。
(2)将反应后的混合物加水稀释到100mL并除去不溶物,加入足量锌粉放出标准状况下5.376L氢气,则原浓硫酸的物质的量浓度为_____,反应的Zn的质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 漂白粉溶液漂白的原理是与空气中的CO2反应生成次氯酸
B. 84消毒液的主要成分是次氯酸钠
C. 金属钠保存在煤油中
D. 久置氯水酸性会减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1
回答下列问题:
(1)反应Ⅱ的△H2=______________。
(2)反应Ⅲ能够自发进行的条件是__ (填“较低温度”、“ 较高温度”或“任何温度”)
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是________。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应Ⅰ,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是____。
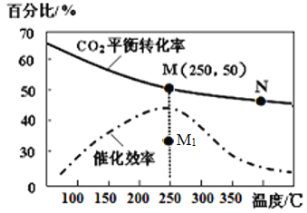
A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入3molH2和1molCO2发生反应Ⅰ,250℃时反应的平衡常数K=__________;若要进一步提高甲醇积分数。可采取的措施有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 乙醇能使酸性高锰酸钾溶液褪色,被氧化生成CO2和H2O
B. ![]() 和C4Hl0的二氯代物的数目不同(不含立体异构)
和C4Hl0的二氯代物的数目不同(不含立体异构)
C. 乙烯能使溴水褪色、能使酸性KMnO4溶液褪色,它们发生反应的类型不同
D. 植物油通过氢化可以变成脂肪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①KClO3 + HCl-----Cl2↑+ KCl + H2O
②Cl2+2KI═2KCl+I2
③I2+5Cl2+6H2O═2HIO3+10HCl
回答下列问题:
(1)反应③中氧化产物是__________(填化学式)
(2)配平反应①并用单线桥法表示该反应中电子转移的方向和数目___KClO3 + ___HCl=_____Cl2↑+____ KCl + ____H2O,______________。
(3)下列说法正确的是______。
A. 反应③中氧化剂和还原剂的物质的量之比为1:5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl-> I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(4)实验室用反应①可以制取Cl2,若反应消耗24.5g KClO3,则至少需用________mL 6mol/LNaOH溶液吸收产生的氯气。写出吸收氯气的离子方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学用含有少量泥沙、CaCl2、MgCl2、Na2SO4的粗盐制取纯净的NaCl,实验前他们设计了如图方案(框图)
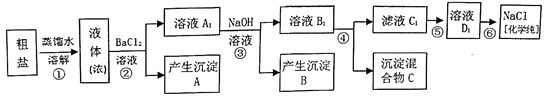
(1)请写出操作第④步所加试剂名称及第②步操作名称:
④_____________________,②___________________________。
(2)写出第⑤步操作中可能发生反应的离子方程式:____________________。
(3)如何检验第②步操作中硫酸根离子已完全除尽:_____________________。
(4)你认为该设计里哪些步骤调换后不影响实验结果:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 由反应SiO2+2C ![]() Si+2CO↑,可得出C的非金属性强于Si
Si+2CO↑,可得出C的非金属性强于Si
B. 由分子组成的物质中一定存在共价键
C. 对于平衡2HI(g)![]() I2(g)+H2(g),压缩容器体积,平衡不移动,气体的颜色不变
I2(g)+H2(g),压缩容器体积,平衡不移动,气体的颜色不变
D. 水的电离是吸热过程,升高温度,水的离子积增大、pH减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com