
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol/L | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O${\;}_{8}^{2-}$)/mol/L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
分析 (1)根据图表已知物理量判断;
(2)根据浓度与时间的关系对比后得出规律再计算;
(3)根据温度与反应速率的关系判断;
(4)根据图表中物理量对比得出结论.
解答 解:(1)图表中的物理量是反应物浓度与时间,通过分析知,反应物的浓度与时间成反比,浓度的变化量与时间的比值为速率,所以得出反应物浓度与反应速率的关系.
故答案为:研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)对比数据组①和②,可以看到,c (S2O82-)不变,c (I-)增大到2倍时,反应时间缩短了一半,即反应速率加快了一倍;
对比实验①和⑤,实验⑤的c (I-)为实验①的3倍,而c (S2O82-)保持不变,则由此可计算实验⑤的反应时间应为实验①反应时间的$\frac{1}{3}$,即t1=88s×$\frac{1}{3}$=29.3s
(3)温度越高,化学反应速率越快,所用时间越短,故选A.
(4)对比数据组①和②,可以看到,c (S2O82-)不变,c (I-)增大到2倍时,反应时间缩短了一半,即反应速率加快了一倍;
对比数据组②和③,可以看到,c (I-)不变,c (S2O82-)增大到2倍时,反应时间缩短了一半,即反应速率也加快了一倍;
对比数据组③和④,可以看到,c (S2O82-)增大到2倍时,c (I-)变为1/4倍时,反应时间增大了一倍,即反应速率减慢了一倍;
对比数据组对比数据组①和③,可以看到,c (I-)和c (S2O82-)均增大到2倍时,反应时间为原反应时间的1/4,即反应速率加快了4倍.
可见两个反应物的浓度和反应速率之间的数学关系是:反应物浓度每增加一倍,反应时间就减少一倍,对于两个反应物来说都是如此,可得出结论:反应速率与反应物起始浓度乘积成正比.
故答案为:反应速率与反应物起始浓度乘积成正比或显色时间与反应物起始浓度乘积成反比.
点评 该题图表的分析方法:先比较两组数据的不同点,再分析不同点说明的问题,从而确定它们之间关系.
如:①、②两组数据的不同点是c(I-)和时间,浓度越大,时间越短,浓度的变化量与时间的比值为速率,所以浓度越大,反应速率越快.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH在水中电离:CH3COOH═H++CH3COO- | |
| B. | 乙醇氧化成乙醛的化学方程式:2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | 乙酸与乙醇发生酯化反应:CH3COOH+CH3CH2OH$→_{△}^{催化剂}$CH3COOCH2CH3 | |
| D. | CaCO3高温分解的热化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,△H=+178.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
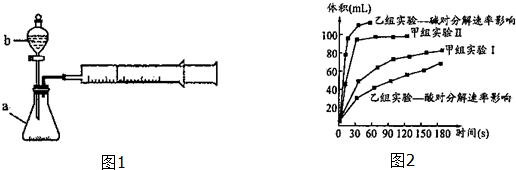
| 实验编号 | 实验目的 | t℃ | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 做实验参照 | 25 | 3滴FeCl3溶液 | 10ml 2%H2O2 |
| 甲组实验Ⅱ | 探究浓度对速率的影响 | 25 | 10ml 5%H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
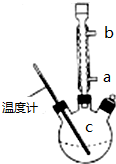
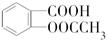 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下: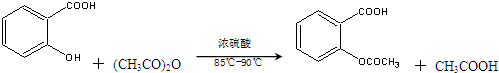
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 难溶电解质的Ksp越小,溶解度就一定越小 | |
| B. | 向含AgCl沉淀的悬浊液中加入NaCl饱和溶液,AgCl的溶解度变小,溶度积常数变小 | |
| C. | 用饱和Na2CO3溶液可以将BaSO4转化为BaCO3,说明Ksp(BaCO3)小于Ksp(BaSO4) | |
| D. | 一般认为沉淀离子浓度小于1.0×10-5 mol/L时,离子就已沉淀完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
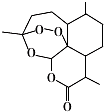
| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素分子结构稳定,受热不易分解 | |
| C. | 青蒿素中含多个环状结构,其中有一个六元碳环 | |
| D. | 青蒿素难溶于水,提取的方法是用有机溶剂萃取后蒸馏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com