
| A. | 用药匙取用粉末状或小颗粒状固体 | |
| B. | 用胶头滴管滴加少量液体 | |
| C. | 给盛有2/3体积液体的试管加热 | |
| D. | 过滤时漏斗的下端管口要紧靠烧杯内壁 |
分析 A.粉末状可利用药匙,小颗粒状固体可利用药匙或镊子取用;
B.胶头滴管可滴加液体;
C.试管中液体不能超过试管容积的$\frac{1}{3}$;
D.下端管口要紧靠烧杯内壁,可使液体沿内壁流下.
解答 解:A.粉末状可利用药匙,小颗粒状固体可利用药匙或镊子取用,则用药匙取用粉末状或小颗粒状固体,故A正确;
B.胶头滴管可滴加液体,1滴液体为0.05mL,则用胶头滴管滴加少量液体,故B正确;
C.试管中液体不能超过试管容积的$\frac{1}{3}$,否则过多液体加热易导致液体溅出,故C错误;
D.下端管口要紧靠烧杯内壁,可使液体沿内壁流下,则过滤时漏斗的下端管口要紧靠烧杯内壁,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验基本操作和实验基本技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
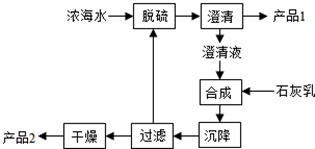
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 若pH>7,则一定是 c${\;}_{{1}_{\;}}$v1=c2v2 | |
| C. | 当pH=7时,若v1=v2,则一定是c2>c1 | |
| D. | 若v1=v2,c2=c1,则 c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeCl3溶液中的Cl- | B. | Na2CO3溶液中的CO32- | ||
| C. | 氯化钡溶液中的Ba2+ | D. | 氟化钠溶液中的F- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol•L-1 | B. | l mol•L-1 | C. | 2 mol•L-1 | D. | 3 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
| A. | 反应开始时,反应速率:甲<乙<丙 | |
| B. | 平衡时,甲中和丙中H2的转化率均是60% | |
| C. | 平衡时,c(CO2)丙=2c(CO2)甲 | |
| D. | 平衡时,乙中CO2的体积分数大于60% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com