
分析 MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,Mn元素的化合价由+4价降低为+2价,生成1molCl2转移2mol电子,该反应中HCl一半为氧化剂,一半作酸,以此计算.
解答 解:根据n=$\frac{N}{{N}_{A}}$=$\frac{6.02×1{0}^{22}}{6.02×1{0}^{23}}$=0.1mol,
设生成氯气的物质的量为x,则
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O~2e-
1 2
x 0.1mol
$\frac{1}{x}$=$\frac{2}{0.1mol}$,解得x=0.05mol,
标准状况下Cl2的体积为0.05mol×22.4L/mol=1.12L,所以参加反应的盐酸的量为:$\frac{4}{n(HCl)}=\frac{2}{0.1}$,所以n(HCl)=0.2mol,
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,4molHCl一半为还原剂被氧化,一半为酸,
则被氧化的HCl为0.1mol,
故答案为:1.12L;0.1mol.
点评 本题考查化学反应方程式的计算,把握反应中元素的化合价的变化分析转移电子及HCl的作用为解答的关键,侧重氧化还原反应计算的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
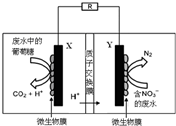
| A. | 电池工作时,既能净化废水,又能发电 | |
| B. | X电极为负极,工作时发生氧化反应 | |
| C. | 正极反应式为2NO3-+10e-+6H2O═N2↑+12OH- | |
| D. | 该电池在常温和高温时都可以工作 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 已知P(红磷,s)=P(白磷,s)△H>0,则白磷比红磷稳定 | |
| B. | 测定相同物质的量浓度的Na2CO3、Na2SiO3的溶液pH,发现后者的更高,说明碳的非金属性强于硅 | |
| C. | 温度和压强一定时,对于可逆反应:2NO2(g)?N2O4(g),混合气体的密度不再改变,则反应达到平衡状态. | |
| D. | 将NaAlO2溶液与NaHCO3溶液混合后生成白色沉淀,是两种溶液水解相互促进的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳钢与生铁主要成分相同,所以性能相同 | |
| B. | 镁铝合金可用于制造飞机、汽车等部件 | |
| C. | 铜合金具有优异的导电、导热性能,但耐腐蚀性能力较差 | |
| D. | 铝铁合金具有很高的熔点,能用于制造火箭外层材料. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在食品袋中放入硅胶、生石灰的透气小袋,可防止食物受潮、氧化变质 | |
| B. | 天然气、酒精和汽油分别属于化石能源、不可再生能源和二次能源 | |
| C. | 富含N、P元素的生活用水可以直接用来灌溉农田 | |
| D. | 酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
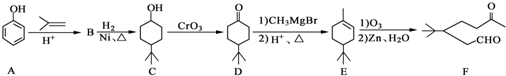
 .
. .同时满足下列条件的B的同分异构体(不包括B)共有11种:能与FeCl3溶液显紫色,苯环上只有两个取代基.
.同时满足下列条件的B的同分异构体(不包括B)共有11种:能与FeCl3溶液显紫色,苯环上只有两个取代基. (任写一种).
(任写一种).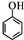 )和CH2=CH2为原料制备有机物
)和CH2=CH2为原料制备有机物  的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com