
 ,B为18电子分子,其结构式为
,B为18电子分子,其结构式为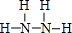 .
.分析 M是地壳中含量最高的金属元素,应为Al;X、Y、Z、L是组成蛋白质的基础元素,有C、N、O、H、P等元素,由于X、Y、Z、L、M五种元素的原子序数依次增大,则X、Y、Z、L分别为H、C、N、O元素,
(1)N、H两元素按原子数目比l:3形成的化合物A为NH3,N、H两元素按原子数目比2:4构成分子B为N2H4,氨气分子中N原子与H原子之间形成1对共用电子对,N2H4分子中N原子之间形成1对共用电子对,N原子与H原子之间形成1对共用电子对;
(2)结合三、四周期容纳元素种数确定与氧原子序数之差,进而计算Se的原子序数;根据最外层电子数分析最高化合价,然后书写最高价氧化物对应的水化物化学式;氨气与氯化氢的反应生成氯化铵;
(3)同主族元素所形成的同一类型的化合物,其结构和性质往往相似,则PH4I与NH4Cl性质相似,根据NH4Cl的性质判断.
解答 解:M是地壳中含量最高的金属元素,应为Al;X、Y、Z、L是组成蛋白质的基础元素,有C、N、O、H、P等元素,由于X、Y、Z、L、M五种元素的原子序数依次增大,则X、Y、Z、L分别为H、C、N、O元素,
(1)N、H两元素按原子数目比l:3形成的化合物A为NH3,N、H两元素按原子数目比2:4构成分子B为N2H4,氨气分子中N原子与H原子之间形成1对共用电子对,其电子式为 ,N2H4分子中N原子之间形成1对共用电子对,N原子与H原子之间形成1对共用电子对,其结构式为
,N2H4分子中N原子之间形成1对共用电子对,N原子与H原子之间形成1对共用电子对,其结构式为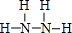 ,
,
故答案为: ;
;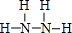 ;
;
(2)Se与O同一主族,Se原子比O原子多两个电子层,即电荷数相差8+18=26,则Se的原子序数为8+26=34,其最高价为+6,最高正价氧化物对应的水化物化学式为H2SeO4;Z的氢化物为氨气,与氯化氢相遇时反应生成氯化铵,有白烟生成,
故答案为:34;H2SeO4;有白烟生成;
(3)同主族元素所形成的同一类型的化合物,其结构和性质往往相似,则PH4I与NH4Cl性质相似,则
A.PH4I与NH4Cl性质相似,都属于离子化合物,故A错误;
B.PH4I与NH4Cl性质相似,具有热不稳定性,加热易分解,分解产物为PH3和HI,HI受热分解得到氢气和紫色的碘蒸气,故B正确;
C.由NH4Cl的性质判断,该化合物能与强碱发生反应生成PH3,故C正确;
D.根据NH4Cl的性质判断,PH3与HI化合可生成PH4I,故D正确;
故答案为:A.
点评 本题考查位置结构与性质关系的应用,题目难度中等,注意根据蛋白质的组成元素结合元素的原子序数关系进行推断,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 22.4L Cl2完全溶液氢氧化钠溶液时,转移电子数为NA | |
| B. | 常温下,18g D2O中所含电子的数目为10NA | |
| C. | 标准状况下,2.24L NH3中含有的共价键数目为0.3NA | |
| D. | 常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO是无色气体 | B. | NO是汽车尾气的有害成分之一 | ||
| C. | 可以用向上排空气法收集NO | D. | NO在一定条件下也可做氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF在水溶液中的电离方程式:HF=H++F- | |
| B. | 醋酸与氢氧化钠反应的离子方程式:H++OHˉ?H2O | |
| C. | NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32ˉ | |
| D. | CuSO4在水溶液中水解的离子方程式:Cu2++2H2O?Cu (OH)2+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
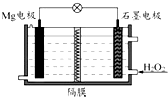 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法错误的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法错误的是( )| A. | 溶液中Cl-向石墨电极移动 | |
| B. | H2O2在石墨电极上发生的电极反应是:H2O2+2e-═2OH- | |
| C. | Mg电极发生氧化反应 | |
| D. | 电子从Mg电极沿导线流向石墨电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 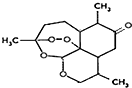 | B. | 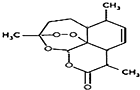 | ||
| C. | 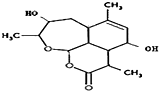 | D. | 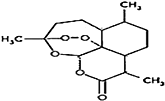 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com