
| A. | C2H6 | B. | C2H4 | C. | C3H6 | D. | C6H10 |
分析 气态烃1mol最多可与1molHCl加成生成氯代烃,说明分子中含有1个C=C,1mol该氯代烃能与5molCl2发生取代反应,说明加成产物分子中含有5个H原子,其中有1个H原子为与HCl加成得到,则原烃分子中含有4个H原子,结合选项判断.
解答 解:气态烃1mol最多可与1molHCl加成生成氯代烃,说明分子中含有1个C=C,1mol该氯代烃能与5molCl2发生取代反应,说明加成产物分子中含有5个H原子,其中有1个H原子为与HCl加成得到,则原烃分子中含有4个H原子,选项中只有C2H4符合,故选:B.
点评 本题以物质的推断为载体,考查了取代反应和加成反应,明确反应时分子组成中的变化是解本题的关键,难度不大.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NO2通入FeSO4溶液中 | B. | CO2通入CaCl2溶液中 | ||
| C. | Cl2通入Na2CO3溶液中 | D. | SO2通入酸化的Ba(NO3)2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学名称为乙醇 | B. | 易挥发 | ||
| C. | 常用作有机溶剂 | D. | 不能被酸性高锰酸钾氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,等质量的SO2和CO2密度比为11:16 | |
| B. | 同温同压下,等质量的SO2和CO2体积比为1:1 | |
| C. | 等物质的量的氢气和氦气在同温同压下具有相等的质子数 | |
| D. | 标准状况下气体摩尔体积就是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
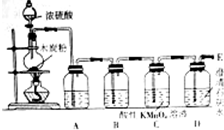 在100mL 18.4mol•L-1浓硫酸中加入1.2g木炭粉,加热使之充分反应.并按如图的装置图进行实验,依次检验反应得到的产物,请回答下列问题:
在100mL 18.4mol•L-1浓硫酸中加入1.2g木炭粉,加热使之充分反应.并按如图的装置图进行实验,依次检验反应得到的产物,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

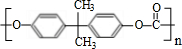 .
.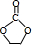 +2CH3OH$\stackrel{一定条件}{→}$CH3OCOOCH3+HOCH2CH2OH.
+2CH3OH$\stackrel{一定条件}{→}$CH3OCOOCH3+HOCH2CH2OH. (写结构简式)
(写结构简式) .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
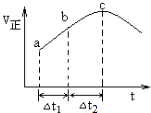
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A. | 少量二氧化碳通入NaClO溶液中:2NaClO+CO2+H2O→Na2CO3+2HClO | |
| B. | 过量的 HCN滴入碳酸钠溶液中 HCN+Na2CO3→NaCN+NaHCO3 | |
| C. | 结合质子能力由强到弱的顺序为:HCO3->CN->C6H5O- | |
| D. | 常温下电离常数:Ka2(H2CO3)>Ka(C6H5OH)>Ka (HCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O2,O3,O4 | B. | 40Ca,40Ar | C. | Fe2+,Fe3+ | D. | 氕,氘,氚 | ||||
| E. | H2O,D2O,T2O | F. | H2,D2,T2 | G. | Na,Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com