
分析 (1)硫在氧气中燃烧,硫被氧气氧化成二氧化硫;
(2)NO和CO催化转化,反应生成CO2和N2;
(3)氨气具有还原性,氧气具有氧化性,氨气中氮元素为-3价,被氧气氧化为+2价的氮元素,所以氨气和氧气反应生成一氧化氮和水;
(4)工业上用氢氧化钙与氯气反应制取漂白粉,据此写出反应的化学方程式;
(5)工业合成氨是氢气和氮气在高温高压催化剂作用下反应生成氨气,反应是可逆反应.
解答 解:(1)硫在氧气中燃烧生成二氧化硫,反应的化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,
故答案为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
(2)在汽车的排气管上装一个催化转化装置,使NO和CO反应,生成CO2和N2,结合原子守恒书写化学方程式为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2,
故答案为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2;
(3)NH3与过量O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水,反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(5)工业合成氨是氢气和氮气在高温高压催化剂作用下反应生成氨气,反应是可逆反应,反应的化学方程式为:N2+3H2$?_{高温高压}^{催化剂}$2NH3,
故答案为:N2+3H2$?_{高温高压}^{催化剂}$2NH3.
点评 本题考查化学方程式的书写,掌握反应原理和书写方法是解答的关键,注意掌握化学方程式的书写原则,熟悉常见物质的化学性质,题目难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | 35.1g | B. | 11.7 g | C. | 23.4g | D. | 58.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 节假日燃放的五彩缤纷的烟花,和一些金属元素的焰色反应有关 | |
| B. | 硅胶常作实验室和袋装食品等的干燥剂 | |
| C. | 正常雨水的pH是5.6,酸雨的pH大于5.6 | |
| D. | 二氧化硅是现代光纤的原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用含磷洗涤剂 | B. | 用工业污水直接灌溉农田 | ||
| C. | 用O3替代Cl2作饮用水消毒剂 | D. | 含Hg2+的废水直接排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①⑥⑧ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
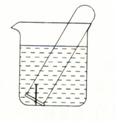 图所示水槽中的试管内有一枚铁钉(含少量的炭),放置数天后观察:
图所示水槽中的试管内有一枚铁钉(含少量的炭),放置数天后观察:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的水溶液可以导电说明是SO2电解质 | |
| B. | 加热NaOH溶液时不能使用玻璃试管,因为玻璃中的SiO2能与NaOH反应 | |
| C. | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,该溶液一定有NH4+ | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-或HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com