
分析 根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量.
令参加反应的氮气的物质的量为nmol,则:
N2 +3H2 ?2NH3 ,
开始(mol):1 3 0
变化(mol):n 3n 2n
平衡(mol):1-n 3-3n 2n
压强之比等于物质的量之比,所以(1-n+3-3n+2n)mol=(1+3)mol×(1-$\frac{1}{10}$),解得n=0.2,以此解答该题.
解答 解:令参加反应的氮气的物质的量为nmol,则:
N2 +3H2 ?2NH3 ,
开始(mol):1 3 0
变化(mol):n 3n 2n
平衡(mol):1-n 3-3n 2n
压强之比等于物质的量之比,所以(1-n+3-3n+2n)mol=(1+3)mol×(1-$\frac{1}{10}$),解得n=0.2,
(1)平衡时n(N2)=(1-n)mol=(1-0.2)mol=0.8mol
平衡时n(H2)=(3-3n)mol=(3-3×0.2)mol=2.4mol
平衡时n(NH3)=2n=0.2mol×2=0.4mol,
则平衡时混合气体中N2、H2和NH3的物质的量之比0.8:2.4:0.4=2:6:1,
故答案为:2:6:1;
(2)2分钟内,NH3的平均反应速率为$\frac{\frac{0.4mol}{2L}}{2min}$=0.1mol/(L﹒min),
故答案为:0.1mol/(L﹒min);
(3)气体的质量不变,则反应前后的气体的摩尔质量之比与物质的量成反比,为(1+3-0.4):(1+3)=9:10,故答案为:9:10.
点评 本题考查化学平衡的有关计算,为高考常见题型,侧重考查学生的分析能力和计算能力,题目涉及主要是反应速率,转化率等概念的理解应用,难度不大,注意基础知识的掌握与三段式解题法的运用.


科目:高中化学 来源: 题型:选择题
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 工业合成氨时采用铁触媒作反应的催化剂 | |
| C. | 工业生产硫酸的过程中使用过量的空气以提高SO2的转化率 | |
| D. | 将收集NO2气体的烧瓶密闭后放在装有热水的烧杯中,发生颜色变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶中有少量蒸馏水 | |
| B. | 溶液从烧杯转移到容量瓶后没有洗涤烧杯 | |
| C. | 未冷却即将溶液转移到容量瓶 | |
| D. | 定容时俯视容量瓶刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
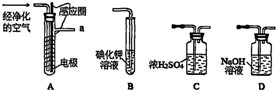
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
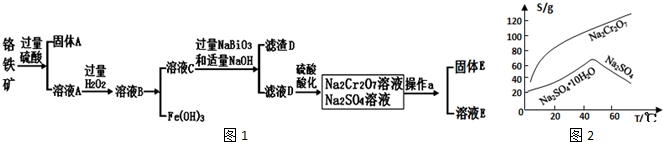
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
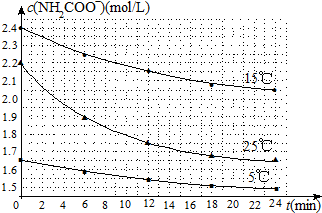
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com