
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如右图,下列说法不正确的是( )。
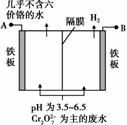
A.A接电源正极
B.阳极区溶液中发生的氧化还原反应为Cr2O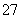 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O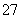 被还原
被还原
科目:高中化学 来源: 题型:
关于工业合成氨的叙述中,错误的是( )
A.在动力、设备、材料允许的情况下,反应尽可能在高压下进行
B.温度越高越有利于工业合成氨
C.在工业合成氨中N2、H2的循环利用可提高其利用率,降低成本
D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铜电极的叙述不正确的是( )
A.在镀件上镀铜时镀件作阴极
B.在镀件上镀铜时可用金属铜作阳极
C.用电解法精炼粗铜时粗铜作阳极
D.用电解法精炼粗铜时纯铜作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能大量共存的是( )
A.Ca2+、HCO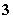 、Cl-、K+
、Cl-、K+
B.Al3+、[Al(OH)4]-、HCO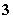 、Na+
、Na+
C.Fe2+、H+、SO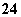 、S2-
、S2-
D.Fe3+、SCN-、Na+、CO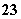
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的①氨水、②氯化铵、③碳酸氢铵、④硫酸氢铵、⑤硫酸铵5种溶液中[NH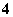 ]的大小顺序是____________________,溶液pH的大小顺序是________________________________________________________________________。
]的大小顺序是____________________,溶液pH的大小顺序是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.1 mol·L-1某一元酸HA)溶液中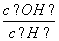 =1.0×10-8。下列叙述正确的是 )。
=1.0×10-8。下列叙述正确的是 )。
A.该溶液中由水电离出的cH+)=1.0×10-3mol·L-1
B.常温下HA的电离平衡常数为1.0×10-6
C.向该HA溶液加水稀释的过程中,cH+)逐渐增大
D.pH=3的HA溶液与pH=11的NaOH溶液等体积混合后,cA-)>cNa+)>cH+)>cOH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,对于反应N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是( )
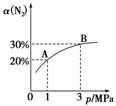
A.将1 mol N2、3 mol H2置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
B.平衡状态由A变到B时,平衡常数K(A)<K(B)
C.上述反应在达到平衡后,增大压强(减小体积),H2的转化率增大
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | |
| A | 稀硫酸 | Na2S | AgNO3与 AgCl的浊液 | Ksp(AgCl)> Ksp(Ag2S) | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3 溶液 | 酸性:硝酸>碳酸>硅酸 |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com