
500℃,在三个相同体积的恒容密闭容器里,分别加入对应物质,甲:2 mol SO2 1 mol O2 乙:2 mol SO2 1 mol O2 1 mol N2 丙 :4 mol SO2 2 mol O2同时进行反应,开始时反应速率最大的是
A、甲 B、乙 C、丙 D、无法判断
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:填空题
(10分)如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
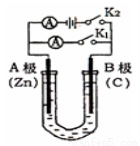
(1)打开K2,合并K1,若所盛溶液为CuSO4溶液:则A为 极,A极的电极反应式为 。若所盛溶液为KCl溶液:则B极的电极反应式为
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是 ,Na+移向 极(填A、B);B电极上的电极反应式为 ,总反应化学方程式是 。
(3)如果要用电解的方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是 (填“粗铜”或“纯铜”),电极反应式是 ,反应一段时间后电解质溶液中Cu2+的浓度将会 (填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高一上学期期中考试化学试卷(解析版) 题型:选择题
下列实验能达到目的的是
A.用溶解、过滤的方法分离CaCl2和NaCl固体混合物
B.向某溶液中加入氢氧化钠固体,加热若产生能使湿润的蓝色石蕊试纸变红的气体,则该溶液中含有NH4+
C.用萃取分液的方法除去酒精中的水
D.用可见光束照射以区别溶液和胶体
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
反应C (s) + H2O (g) ? ?CO (g) + H2(g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是
?CO (g) + H2(g)在一可变容积的密闭容器中进行,下列条件的改变能加快其反应速率的是
A.保持体积不变,充入N2使体系压强增大
B.增加C的量
C.保持压强不变,充入N2 使容器体积变大
D.将容器的体积缩小一半
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
则25 ℃时,反应X+3Y? ?2Z的平衡常数为
?2Z的平衡常数为
A.500 B.600 C.1 200 D.1 600
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:填空题
(本题6分)依据某氧化还原反应设计的原电池如图所示。
(1)该氧化还原反应的离子方程式为_________________________________。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出铜片和银片洗净干燥后称重,总质量为67.6g,请计算:通过导线的电子的物质的量。(要求有计算过程)

查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)? ?4NO2(g)+O2(g) ΔH>0
?4NO2(g)+O2(g) ΔH>0
T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500 s内N2O5分解速率为2.96×10-3 mol·(L·s)-1
B.T1温度下的平衡常数为K1=125, 1000 s时转化率为50%
C.其他条件不变时,T2温度下反应到1000 s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
D.T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.不用稀硫酸而用浓硫酸
C.滴加少量CuSO4溶液 D.不用铁片而用铁粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com