

���� ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ǰ7��Ԫ�ش��ڵڶ����ڣ���7��Ԫ�ش��ڵ������ڣ���ԭ��������֪��XΪOԪ�أ�YΪFԪ�أ�ZΪNa��MΪAl��NΪSi��RΪCl��
��� �⣺ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ǰ7��Ԫ�ش��ڵڶ����ڣ���7��Ԫ�ش��ڵ������ڣ���ԭ��������֪��XΪOԪ�أ�YΪFԪ�أ�ZΪNa��MΪAl��NΪSi��RΪCl��
��1��NΪSi����Ԫ�����ڱ��е�λ�ã���3���ڢ�A�壬�ʴ�Ϊ����3���ڢ�A�壻
��2��ͬ�����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶��Na��Al��O��F��
�ǽ�����Cl��Si��������������ˮ��������ԣ�HClO4��H2SiO3��
�ʴ�Ϊ��Na��Al��O��F��HClO4��H2SiO3��
��3��Z��X�γɵĺ��зǼ��Լ������ӻ�����Ϊ�������ƣ�����ʽΪ��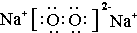 ��
��
�ʴ�Ϊ��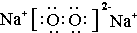 ��
��
��4����֪1mol Na��ˮ��Ӧ���ָ������£��ų�283.5kJ��������Na��ˮ��Ӧ���Ȼ�ѧ��Ӧ����ʽ��2Na��s��+2H2O��l��=2NaOH��aq��+H2��g����H=-567 kJ/mol��
�ʴ�Ϊ��2Na��s��+2H2O��l��=2NaOH��aq��+H2��g����H=-567 kJ/mol��
���� ���⿼��λ�ýṹ���ʵĹ�ϵ��Ӧ�ã���Ŀ�Ѷ��еȣ��ƶ�Ԫ���ǽ���Ĺؼ�������ԭ�Ӱ뾶�仯���ɽ��ԭ�����������ƶϣ�����������Ҫץס������������Ԫ�ء������֣�


 ���ſ����ϵ�д�
���ſ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3-+OH-��CO32-+H2O | |
| B�� | Ba2++OH-+HCO3-��BaCO3��+H2O | |
| C�� | Ba2++2OH-+2HCO3-��BaCO3��+CO32-+H2O | |
| D�� | 2Ba2++3OH-+3HCO3-��2BaCO3��+CO32-+3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ҫ�ɷ�ΪNa2CO3 | B�� | �ȵĴ�����Һȥ��Ч������ | ||
| C�� | ��������������ˮ�� | D�� | �����������θ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
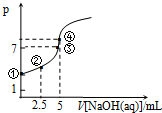 ��������10mL 0.1mol•L-1HN3�������ᣩ��Һ����εμ�0.2mol•L-1��NaOH��Һ����ҺpH�ı仯������ͼ��ʾ����Һ���ʱ����ı仯���¶Ⱥ��Բ��ƣ�HN3��Ka=10-4.7��������˵������ȷ���ǣ�������
��������10mL 0.1mol•L-1HN3�������ᣩ��Һ����εμ�0.2mol•L-1��NaOH��Һ����ҺpH�ı仯������ͼ��ʾ����Һ���ʱ����ı仯���¶Ⱥ��Բ��ƣ�HN3��Ka=10-4.7��������˵������ȷ���ǣ�������| A�� | ˮ�������c��OH-�����ٵ�С�� �۵� | |
| B�� | �˷�Ӧ�ĵζ�ʵ����ѡ�ü�����ָʾ�� | |
| C�� | �ڵ�ʱc��N3-����c��Na+����c��HN3����c��H+����c��OH-�� | |
| D�� | �ܵ�ʱc��Na+��=c��N3-��+c��HN3��=$\frac{1}{15}$mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʵ��ʱ��������ƿ�з��뼸����ʯ�������Ƭ�� | |
| B�� | �������Ż�ʱʹ����ĭ�������� | |
| C�� | ���Թܼ���̼�����ƹ���ʱʹ�Թܿ���������б | |
| D�� | Ũ���ὦ��Ƥ����������ϡ����������Һ��ϴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol/L NH4HCO3��Һ�У�K+��Na+��NO3-��Cl- | |
| B�� | $\frac{{k}_{W}}{c��{H}^{+}��}$=1��10-13 mol/L����Һ�У�NH4+��Na+��SiO32-��Cl- | |
| C�� | ��Al��Ӧ�ܷų�H2����Һ�У�Fe2+��K+��NO3-��SO42- | |
| D�� | ˮ�����c��H+��=1��10-13mol/L����Һ�У�K+��Na+��AlO2-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʹʯ����Һ�ʺ�ɫ����Һ�У�Na+��SO42-��Fe3+��MnO4-���Դ������� | |
| B�� | NA���������ӵ���������ֵ��1 mol������ؾ����������������������ΪNA | |
| C�� | 235U��238U���ת�����ǻ�ѧ�仯 | |
| D�� | Ԫ��O��S��P����̬�⻯�����ȶ���������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �Ҷ����������ᣬ�����ǻ�ѧѧϰС���ͬѧ�Բ��ᾧ�壨H2C2O4•xH2O�����е�̽����ѧϰ�Ĺ��̣�������벢Э������������ѧϰ������ͬѧ���о������ǣ�̽���ⶨ���ᾧ�壨H2C2O4•xH2O����xֵ��ͨ���������Ϻ������Ѱ�ã�����������ˮ��ˮ��Һ����������KMnO4��Һ���еζ���2MnO${\;}_{4}^{-}$+5H2C2O4+6H+�T=2Mn2++10CO2��+8H2OѧϰС���ͬѧ����˵ζ��ķ����ⶨxֵ��
�Ҷ����������ᣬ�����ǻ�ѧѧϰС���ͬѧ�Բ��ᾧ�壨H2C2O4•xH2O�����е�̽����ѧϰ�Ĺ��̣�������벢Э������������ѧϰ������ͬѧ���о������ǣ�̽���ⶨ���ᾧ�壨H2C2O4•xH2O����xֵ��ͨ���������Ϻ������Ѱ�ã�����������ˮ��ˮ��Һ����������KMnO4��Һ���еζ���2MnO${\;}_{4}^{-}$+5H2C2O4+6H+�T=2Mn2++10CO2��+8H2OѧϰС���ͬѧ����˵ζ��ķ����ⶨxֵ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com