
分析 以钛铁矿(含 85%的FeTiO3,杂质不参与反应)为原料制备Ti的工艺:用浓硫酸处理钛铁矿,产物是TiOSO4和 FeSO4,该反应为非氧化还原反应,则发生的反应为:2H2SO4+FeTiO3=FeSO4+TiOSO4+2H2O,然后加水,TiOSO4 遇水水解,过滤得到H2TiO3,H2TiO3加热灼烧得到TiO2,加入氯气、过量碳高温加热反应生成TiCl4和一氧化碳,四氯化钛和金属镁高温加热反应得到氯化镁和钛金属,据此分析作答.
解答 解(1)钛酸亚铁FeTiO3中铁元素+2价,氧元素-2价,化合物中化合价代数和为0,则钛元素+4价,由题可知,硫酸与 FeTiO3反应产物是TiOSO4和 FeSO4,该反应为非氧化还原反应,则化学方程式为2H2SO4+FeTiO3=FeSO4+TiOSO4+2H2O;
故答案为:2H2SO4+FeTiO3=FeSO4+TiOSO4+2H2O;
(2)TiOSO4 遇水水解,TiO2++2H2O?H2TiO3+2H+,加热,加水稀释,均可促进平衡正向移动生成H2TiO3,
故答案为:TiO2++2H2O?H2TiO3+2H+,加热,加水促进平衡正向移动;
(3)TiCl4极易水解,将它暴露在空气中会产生烟雾,生成二氧化钛和氯化氢气体,发生的反应为:TiCl4+2H2O=TiO2+4HCl;
故答案为:TiCl4+2H2O=TiO2+4HCl;
(4)活泼金属钠可以将金属钛置换出来:TiCl4+4Na$\frac{\underline{\;高温\;}}{Ar}$Ti+4NaCl,Zn、和Fe都是不可以的,活泼性差;
故答案为:TiCl4+4Na$\frac{\underline{\;高温\;}}{Ar}$Ti+4NaCl;
(5)准确滴加氯化铁溶液可使用滴定管,氯化铁有较强的氧化性,应用酸式滴定管;
设滤液Ti3+的物质的量为X.
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
1 1
X 0.1000mol•L-1×0.03L
解得X=0.1000mol•L-1×0.03L=0.003mol
则待测钛液中TiOSO4的物质的量=0.003mol×5=0.015mol
根据C=$\frac{0.015mol}{0.01L}$=1.50 mol•L-1;
故答案为:酸式滴定管;1.50 mol•L-1.
点评 本题以框图推断的形式结合化学实验和元素化合物的相关知识考查学生的阅读、分析、提取信息解决问题的能力,主要是化学工艺流程,题目难度较大,做题时注意从物质的性质角度结合题中信息解答.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 | |
| B. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 | |
| C. | 浓硫酸可用于干燥H2S和CO2 | |
| D. | 合金的物理性质一般与其各组分金属的物理性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
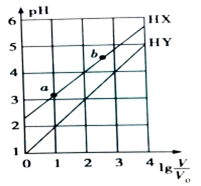 常温下,浓度均为0.1mol•L-1、体积均为V0的HX和HY溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示(不考虑HX、HY和H2O的挥发),下列叙述正确的是( )
常温下,浓度均为0.1mol•L-1、体积均为V0的HX和HY溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示(不考虑HX、HY和H2O的挥发),下列叙述正确的是( )| A. | HX和HY都是弱酸,且HX的酸性比HY的弱 | |
| B. | HX的电离程度:a点大于b点 | |
| C. | HX溶液由a点稀释至b点时,由水电离出的c(H+)•c(OH-)不变 | |
| D. | 当lg$\frac{V}{{V}_{0}}$=3时,若两溶液同时升高温度,则$\frac{c({X}^{-})}{c({Y}^{-})}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,将pH=3的盐酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 | |
| B. | 25℃时Ksp(AgCl)=1.8×10-10,向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度可能减小 | |
| C. | 浓度均为0.1mol•L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>NaHCO3>(NH4)2SO4>NH4Cl | |
| D. | 为确定H2A是强酸还是弱酸,可测0.1mol•L-1NaHA溶液的pH,若pH>1,则H2A是弱酸;若pH=1,则H2A是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,3.36L氧气与2.4g碳反应,生成CO2分子数为0.2NA | |
| B. | 标准状况下,1.12LCl2发生反应转移的电子数一定为0.1NA | |
| C. | lL0.lmol•L-1氨水中NH3•H2O分子数为0.1NA | |
| D. | 10g46%酒精(C2H5OH)中含氧原子总数大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯锌与稀硫酸反应时,加少量CuSO4溶液,可使反应速率加快 | |
| B. | 甲烷和氧气以及KOH溶液构成的新型燃料电池中,负极上发生的反应为CH4+8OH-+8e-═CO2+6H2O | |
| C. | 把铜片和铁片紧靠在一起浸入稀H2SO4中,铁片表面出现气泡 | |
| D. | 把铜片插入FeCl3溶液中,在铜片表面出现一层铁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com