
| A. | 所占的体积相同 | B. | 密度相同 | ||
| C. | 所含原子数目相同 | D. | 所占体积一定是22.4L |
分析 A.同温同压下,分子数相同的气体,它们的体积相等;
B.同温同压下,气体的密度之比等于相对分子质量之比;
C.结合分子式计算原子数目之比;
D.二者物质的量不确定,且不一定为标况下.
解答 解:A.同温同压下,气体分子间距约相等,气体分子大小可以忽略不计,故分子数相同的氨气和氢气占有的体积相等,故A正确;
B.同温同压下,气体的密度之比等于相对分子质量之比,氨气和氢气的密度之比为17:2,故B错误;
C.分子数相同的氨气和氢气含有原子数目之比为4:2=2:1,故C错误;
D.二者物质的量不确定,且不一定为标况下,不能确定它们的体积,故D错误,
故选:A.
点评 本题考查阿伏伽德罗定律及其推论,难度不大,注意根据PV=nRT理解阿伏伽德罗定律及其推论.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
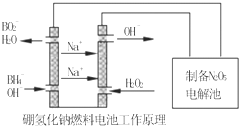 二甲基亚砜有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下
二甲基亚砜有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下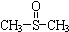 生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜,有关反应如下:
生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜,有关反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中共价键越强,熔沸点越高 | |
| B. | 只含共价键的物质,一定是共价化合物 | |
| C. | HF的分子间作用力大于HCl,故HF比HCl更稳定 | |
| D. | 分子晶体中,可能不存在共价键,但一定存在分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | Ag | C. | Cl2 | D. | O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
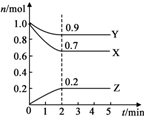 某温度时,在2L的密闭容器中,X、Y、Z三种气体物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种气体物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c=$\frac{ρ•w}{M}$ | B. | c=$\frac{ρ•M}{w}$ | C. | c=$\frac{M}{m•V}$ | D. | c=$\frac{m}{M•V}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3具有还原性 | B. | 液氨、氨气、氨水是同一种物质 | ||
| C. | 氨气是非电解质,氨水是电解质 | D. | 氨水的主要成分是NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com