
| A、若①正确,则溶液中溶质一定为NH4Cl |
| B、若③正确,则溶液中c(NH3?H2O)+c(NH4+)>c(Cl-) |
| C、若④正确,且该溶液是由盐酸和氨水等体积混合而成,则盐酸中c(H+)等于氨水中c(OH-) |
| D、上述四种关系式均可能成立 |


科目:高中化学 来源: 题型:
| A、常温常压下,71gCl2和73gHCl中所含氯原子都是2NA |
| B、在非标准状况下,1mol任何气体的体积不可能是22.4L |
| C、标准状况下,22.4LH2和O2的混合气体中含分子总数为2NA |
| D、10℃时,1molO2的体积一定大于22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
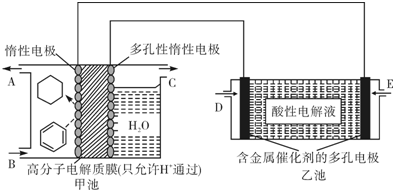
| A、乙池中溶液的pH变大 |
| B、E处通入H2,C处有O2放出 |
| C、甲池中阴极区只有苯被还原 |
| D、导线中共传导11.2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+):c(OH-)=1:10-2的溶液中K+、Ba2+、ClO-、CO32-一定能大量存在 | ||
| B、水电离出来的c(H+)=10-13mol/L的溶液中K+、Cl-、NO3-、I-一定能大量存在 | ||
C、往0.1mol/LCH3COOH溶液中通人少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中
| ||
| D、等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3⑤NH4HCO3中c(CO32-)的大小关系为:②>④>③>⑤>① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
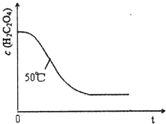 某小组利用H2C204溶液和酸性KMn04溶液反应来探究“条件对化学反应速率的影响”.
某小组利用H2C204溶液和酸性KMn04溶液反应来探究“条件对化学反应速率的影响”.| 实验序号 | 反应温度/℃ | H2C2O4溶液 | 酸性KMnO4溶液 | H2O | ||
| V/mL | c/(mol?L-1) | V/mL | c/(mol?L-1) | V/mL | ||
| ① | 25 | 8.0 | 0.20 | 5.0 | 0.010 | 0 |
| ② | 25 | 6.0 | 0.20 | 5.0 | 0.010 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:
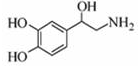
| A、每个去甲肾上腺素分子中含有3个酚羟基 |
| B、1mol去甲肾上腺素最多能与2molBr2 |
| C、甲肾上腺素分子不能与饱和的碳酸氢钠溶液发生反应 |
| D、去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com