
 短周期元素X、Y、Z、W在周期表中的位置关系如右图所示,已知在同周期元素的常见简单离子中,W的简单离子半径最小,X、Y、Z、W的单质及其化合物在日常生活中用途极其广泛.
短周期元素X、Y、Z、W在周期表中的位置关系如右图所示,已知在同周期元素的常见简单离子中,W的简单离子半径最小,X、Y、Z、W的单质及其化合物在日常生活中用途极其广泛.| X | Y | Z | |
| W |
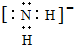 .
.分析 由短周期元素X、Y、Z、W在周期表中的位置可知,X、Y、Z处于第二周期,W处于第三周期,在同周期元素的常见简单离子中,W的简单离子半径最小,则W为Al,可推知X为C、Y为N、Z为O.
(1)主族元素周期数=电子层数、主族族序数=最外层电子数;
(2)液态NH3与液态H2O可以发生类似方式电离,则液态NH3中电离得到NH4+、NH2-;
(3)Al2O3、N2、C在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:1,反应生成AlN与CO;
(4)氯离子会破坏铝表面氧化膜;
(5)该装置是原电池,负极上一氧化碳失电子发生氧化反应,电极反应式为CO-2e-+O2-═CO2,正极上氧气得电子发生还原反应,原电池放电时电子从负极流向正极,阴离子向负极移动,一氧化碳的含量越大,原电池放电时产生的电流越大;
(6)由元素C与元素O组成的某种阴离子具有还原性,能被酸性KMnO4氧化,该阴离子为C2O42-,利用化合价升降相等及原子守恒、电荷守恒进行配平.
解答 解:由短周期元素X、Y、Z、W在周期表中的位置可知,X、Y、Z处于第二周期,W处于第三周期,在同周期元素的常见简单离子中,W的简单离子半径最小,则W为Al,可推知X为C、Y为N、Z为O.
(1)X为C元素,原子核外有2个电子层、最外层电子数为4,处于周期表中第二周第ⅣA族,
故答案为:第二周第ⅣA族;
(2)液态NH3与液态H2O可以发生类似方式电离,则液态NH3中电离得到NH4+、NH2-,NH2-中N原子与H原子之间形成1对共用电子对,其电子式为: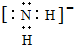 ,
,
故答案为: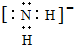 ;
;
(3)Al2O3、N2、C在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:1,反应生成AlN与CO,反应方程式为:Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$2AlN+3CO,
故答案为:Al2O3+N2+3C $\frac{\underline{\;高温\;}}{\;}$2AlN+3CO;
(4)氯离子会破坏铝表面氧化膜,铝容器不能用来腌制咸菜,故答案为:氯离子会破坏铝表面氧化膜;
(5)该装置是原电池,负极上一氧化碳失电子发生氧化反应,电极反应式为CO-2e-+O2-═CO2,
A.工作时电极b通入空气,b作正极,阴离子向负极移动,O2-由电极b流向电极a,故A正确;
B.原电池放电时电子从负极流向正极,故电流由电极b通过传感器流向电极a,故B错误;
C.一氧化碳的含量越大,原电池放电时产生的电流越大,故C正确,
故答案为:CO-2e-+O2-═CO2;AC;
(6)由元素C与元素O组成的某种阴离子具有还原性,能被酸性KMnO4氧化,该阴离子为C2O42-,反应中C元素化合价由+3升高为+4,共升高2价,Mn元素化合价由+7降低为+2,共降低5价,化合价升降最小公倍数为10,故C2O42-的系数为5,MnO4-的系数为2,由原子守恒可知:CO2的系数为10,Mn2+的系数为5,H2O为8,H+的系数为16,故配平后离子方程式为:5C2O42-+2MnO4-+16H+═10CO2+2Mn2++8H2O,
故答案为:5、C2O42-、2、16、10、2、8.
点评 本题考查结构性质关系应用,涉及电子式、原电池、氧化还原反应配平等,推断应是解题关键,侧重对学生综合能力与基础知识的掌握.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,判断下列物质不能与B发生化学反应的有C.
,判断下列物质不能与B发生化学反应的有C.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2分子的比例模型: | |
| B. | 过氧化氢的电子式: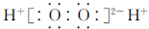 | |
| C. | 氟原子的结构示意图: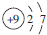 | |
| D. | H2CO3的电离方程式:H2CO3?2H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
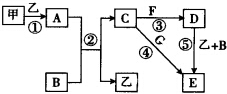 下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物.B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色.
下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物.B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 分子模型可以直观地表现分子结构的特点.如图表示某烃分子的一种模型,有关说法中正确的是( )
分子模型可以直观地表现分子结构的特点.如图表示某烃分子的一种模型,有关说法中正确的是( )| A. | 该图表示的是乙烯分子的球棍模型 | |
| B. | 该烃分子是非极性分子 | |
| C. | 该烃的电子式为: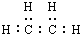 | |
| D. | 该烃分子中半径较大的原子其核外电子排布的轨道表示式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用装置制备Fe(OH)2并能较长时间观察其颜色 | |
| B. |  用装置制备并收集少量氨气 | |
| C. |  用装置除去H2S中的水蒸气 | |
| D. |  用装置制取纯净的乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
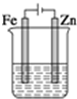
| A. | 溶液中氯离子向锌电极移动 | B. | 锌电极上生成氧化产物 | ||
| C. | 两端电极产生相等体积的气体 | D. | 电路中电子转移数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
.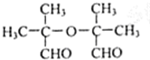 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com