
�����ң���Ҫ�ɷ�ΪAl��Al2O3����������CuO��SiO2��FeO��Fe2O3���ʣ�Ϊԭ�ϣ����Ƶ�Һ��ۺ��Ȼ���Alm��OH��nCl3m-n�������IJ��ֹ�������ͼ��ʾ�����ֲ���Ͳ�������ȥ����

��֪ijЩ������������±���

��1������I�� ��Al2O3�����ᷴӦ�����ӷ���ʽ�� ��
��2������2Ϊ��ɫ���ú�ɫ���ʵĻ�ѧʽ�� ��
��3������Һ2�м���NaClO��Һ�����ٲ������ɫ��������ʱ��Һ��pHԼΪ3��7��NaClO�������� ��
��4������Һ3��pH����4��2��4��5������ˮ�ⷴӦ�õ�Һ��ۺ��Ȼ�������Ӧ�Ļ�ѧ����ʽ�� ��
��5������Һ3���Ҳ���Եõ�Һ��ۺ��Ȼ�����װ����ͼ��ʾ�������ӽ���Ĥֻ����������ͨ�����缫Ϊ���Ե缫����

��д�������ҵĵ缫��Ӧ�� ��
�ڼ����ڷ�Ӧ�������ɾۺ���������ԭ���� ��
��1������ ��2�֣�Al2O3+6H+=2Al3++3H2O (2��)
��2��CuS (2��)
��3����Fe2+����ΪFe3+��ʹת��ΪFe��OH��3���� ��2�֣�
��4��mAlCl3+nH2O=Alm��OH��nCl3m-n+nHCl (д��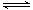 ���÷�)��1�֣�
���÷�)��1�֣�
��5����2H++2e-=H2�� (2��)
�ڵ������з�Ӧ���е�Cl-ͨ�������ӽ���Ĥ���������ң��������е�OH-ͨ�������ӽ���Ĥ���뷴Ӧ�ң����ɾۺ��Ȼ�������2�֣�
��������
�����������1������ϡ�����CuO��SiO2������ϡ��������ʿɹ��˳������Բ���I�ǹ��ˣ���������ϡ���ᷴӦ�����ӷ���ʽΪAl2O3+6H+=2Al3++3H2O��
��2��������������ʿ�֪�ú�ɫ����ΪCuS����Ϊ��������Һϡ�����У�
��3�������������Ŀ���ǰ��������������������ӣ�ת��ΪFe��OH��3������ȥ��
��4�����ݾۺ��Ȼ����Ļ�ѧʽ�������غ㶨�ɣ��Ȼ���ˮ��Ļ�ѧ����ʽΪ
mAlCl3+nH2O=Alm��OH��nCl3m-n+nHCl��
��5������Һ3����Ҫ�ɷ����Ȼ������������ӷŵ�˳���������������ӷŵ磬����ӦΪH+�ŵ磬�缫��ӦΪ2H++2e-=H2����
�ڷ�Ӧ�������Ϊ�����ӽ���Ĥ���������з�Ӧ���е�Cl-ͨ�������ӽ���Ĥ���������ң���������OH-Ũ������ͨ�������ӽ���Ĥ���뷴Ӧ�ң����ɾۺ��Ȼ�����
���㣺���黯ѧ�뻯����������ϵ������Ŀ��Ϣ�ķ�������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
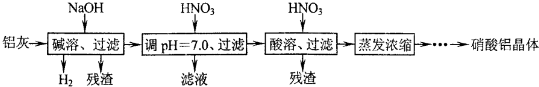
| Al��OH��3 | ��ʼ���� | ������ȫ | ������ʼ�ܽ� | ������ȫ�ܽ� |
| pH | 3.3 | 5.0 | 7.8 | 12.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| �� |
| 143.5 |
| �� |
| 143.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���Ϻ����ɽ����и߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
�ۺ�����PAC����һ������Ч�����߷������������㷺����ˮ�Ĵ����������ҡ�������������Ϊԭ�ϣ���Ҫ�ɷ�ΪAl��Al2O3������ȡ�ۺ�����ʵ�鲽�����£�
�ۺϹ�����Ҫ������Al3+�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�꽭��ʡ�Ͼ��γ��и߿���ѧ��ģ�Ծ��������棩 ���ͣ������
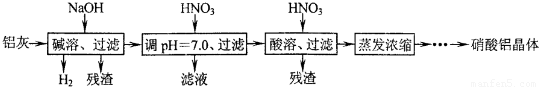
| Al��OH��3 | ��ʼ���� | ������ȫ | ������ʼ�ܽ� | ������ȫ�ܽ� |
| pH | 3.3 | 5.0 | 7.8 | 12.8 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com