
| A、乙醇、乙酸、乙酸乙酯都能发生取代反应 |
| B、乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
| C、乙烯和聚乙烯中均含有不饱和碳碳双键 |
| D、淀粉和蛋白质都是高分子化合物 |
 中不含有不饱和碳碳双键,故C错误;
中不含有不饱和碳碳双键,故C错误;

科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将少量AgNO3溶液滴入氨水中:Ag++2NH3?H2O═[Ag(NH3)2]++2H2O |
| B、将少量SO2通入NaClO溶液中:SO2+2ClO-+H2O═SO32-+2HClO |
| C、澄清石灰水与稀硝酸反应:Ca(OH)2+2H+═2H2O+Ca2+ |
| D、水玻璃长时间放置在空气中:SiO32-+CO2═H2SiO3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、盐桥的作用是让电子通过,以构成闭合回路 |
| B、总反应为:2H++Zn═H2+Zn2+且△H<0 |
| C、随着反应进行,右烧杯中溶液pH变小 |
| D、随着反应进行,左烧杯溶液中的SO42-向右烧杯迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在H2O2溶液中加入少量MnO2粉末 |
| B、将一小块铝片投入足量NaOH溶液中 |
| C、将少量氢氧化铝加入足量的浓氨水中 |
| D、常温下将一小块铁片投入足量的浓硝酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2、Na2CO3 |
| B、NaOH、Na2CO3 |
| C、Na2CO3 |
| D、Na2O2、NaOH、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铝熔点很高,可制造用于熔融烧碱的坩埚 |
| B、炭具有还原性,一定条件下能将二氧化硅还原为硅 |
| C、常温下二氧化硅不与强酸反应,可用石英容器盛放氢氟酸 |
| D、SO2具有漂白性,可用作熏蒸粉丝使其增白 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、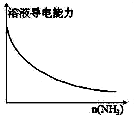 向一定量的CH3COOH溶液中通入NH3至过量 |
B、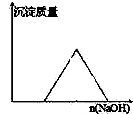 向等物质的量的HCl和AlCl3溶液中滴入NaOH溶液至过量 |
C、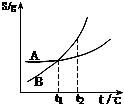 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液升温至t2℃时,溶质的质量分数B=A |
D、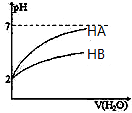 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com