
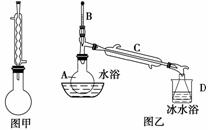
苯甲酸甲酯是一种重要的香料。其合成装置为
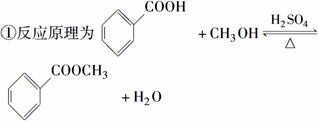
②反应物和产物的部分性质如下表所示:
| 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
| 苯甲酸 | 249 | 1.265 9 | 微溶于水 |
| 甲醇 | 64.6 | 0.791 0 | 易溶于水 |
| 苯甲酸甲酯 | 198 | 1.090 0 | 不溶于水 |
③实验步骤如下:
步骤一:在干燥的圆底烧瓶(如图甲)中加入12.20 g苯甲酸和12.10 mL甲醇。边缓缓摇动边加入3 mL浓硫酸,再加上几粒固体X,装上冷凝管,加热。
步骤二:取下图甲所示冷凝管,在烧瓶上安装图乙所示的装置,利用热水浴加热烧瓶;一段时间后,冷却,将烧瓶中溶液倒入分液漏斗中,先用水洗涤,再用浓碳酸钠溶液洗涤即得粗苯甲酸甲酯。
步骤三:将苯甲酸甲酯重新加入图乙所示装置中,加热,收集一定温度下的馏分,即得纯净的苯甲酸甲酯,质量为8.84 g。
回答下列问题:
(1)步骤一中固体X的作用是防止暴沸,X的名称是________________________。
(2)图甲装置中冷凝管的作用是________________________________________。
(3)图乙装置中仪器A的名称是________,仪器D的名称是________。
(4)步骤二中热水浴的目的是______________________,在分液漏斗中用水洗涤的目的是__________________,用碳酸钠洗涤的目的是______________________。
(5)步骤三中收集的馏分温度范围为________。(填正确答案标号)
a.63~66 ℃ b.197~198 ℃
c.248~250 ℃ d.>250 ℃
(6)本实验中,苯甲酸甲酯的产率为________。
答案 (1)沸石 (2)冷凝回流,提高原料利用率
(3)圆底烧瓶 锥形瓶
(4)除去产品中的甲醇 除去残留的甲醇 除去苯甲酸 (5)b (6)65%
解析 (1)由“防止暴沸”的作用可知X为沸石。(2)图甲中的冷凝管为竖直状态,所起作用是使反应物和产物回流,提高原料利用率,减少产物挥发。(3)由装置乙中仪器的作用与装置特点可知A、B、C、D分别为烧瓶、温度计、冷凝管、锥形瓶。(4)由表格中给出的反应物和产物的沸点可知甲醇的沸点较低,用蒸馏的办法可除去产品中的大多数甲醇;甲醇易溶于水,所以水洗涤除去的是甲醇;苯甲酸与碳酸钠反应生成可溶性的苯甲酸钠。(5)产品精制蒸馏收集的是苯甲酸甲酯,由表格中的沸点数据可知应该收集198 ℃的馏分,故选项b正确。(6)甲醇过量,理论上生成的苯甲酸甲酯为12.20 g÷122 g·mol-1×136 g·mol-1=13.6 g,故产率为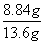 ×100%=65%。
×100%=65%。


科目:高中化学 来源: 题型:
为了说明盐类水解是吸热反应,现用醋酸钠进行实验,表明它在水解时是吸热反应,其中的实验方案正确的是( )
A将CH3COONa·3H2O晶体溶于水,温度降低 B醋酸钠溶液的pH大于7
C醋酸钠溶液滴入酚酞显红色,加热后颜色变深 D醋酸钠溶液与浓H2SO4微热,可逸出醋酸蒸气
查看答案和解析>>
科目:高中化学 来源: 题型:
设计实验证明酸性:CH3COOH>H2CO3>H2SiO3。
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
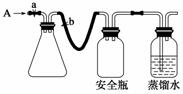
实验室用下列方法测定某水样中O2的含量。
(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为____________________。
再用I-将生成的MnO(OH)2还原为Mn2+,反应的离子方程式为MnO(OH)2+2I-+4H+===Mn2++I2+3H2O。然后用Na2S2O3标准溶液滴定生成的I2,反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是________;
②用注射器抽取某水样20.00 mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸溶液;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入2~3滴________作指示剂;
⑧用0.005 mol·L-1 Na2S2O3滴定至终点。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________(单位:mg·L-1)。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将________(填“偏大”、“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组对加碘食盐中碘酸钾进行研究。
(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
a.称取W g加碘盐,加适量蒸馏水溶解;
b.用稀硫酸酸化,再加入过量KI溶液;
c.以淀粉为指示剂,用物质的量浓度为1.00×10-3 mol·L-1的Na2S2O3标准溶液滴定。
(已知:IO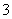 +5I-+6H+===3I2+3H2O,I2+2S2O
+5I-+6H+===3I2+3H2O,I2+2S2O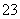 ===2I-+S4O
===2I-+S4O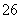 )
)
滴定时Na2S2O3溶液应放在________(填“酸式滴定管”或“碱式滴定管”),滴定至终点时消耗Na2S2O3溶液20.00 mL,其终点颜色变化为________;加碘食盐样品中的碘元素含量是____________mg·kg-1(以含W的代数式表示)。
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
| 顺序 | 步骤 | 实验现象 |
| ① | 取少量纯净的NaCl, 加蒸馏水溶解 | 溶液无变化 |
| ② | 滴加淀粉KI溶液,振荡 | 溶液无变化 |
| ③ | 然后再滴加稀H2SO4溶液,振荡 | 溶液变蓝色 |
请推测实验③中产生蓝色现象的可能原因:__________;根据学生乙的实验结果,请对学生甲的实验结果作出简要评价____________________。
(3)工业上通常用电解KI溶液的方法来制备碘酸钾,电解过程中请你帮助学生丙设计实验来判断电解是否完全。仪器不限,可选的试剂:淀粉溶液、H2O2溶液、稀硫酸。
| 实验操作 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol A气体和2 mol B气体在2 L的容器中混合,并在一定条件下发生如下反应2A(g)+B(g)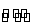 2C
2C (g),若2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
(g),若2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
①用物质A表示反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示反应的平均速率为0.6 mol·L-1·s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol·L-1
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1 mol/L FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值):
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(1)用KSCN溶液检验出Fe3+的现象是________________________。
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应:________________________________________________________________________。
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有________性。
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl溶液的浓度是________mol/L。
②Ⅳ中检验Cl2的实验方法:_________________________________________________。
③与Ⅱ对比,得出的结论(写出两点):________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com