
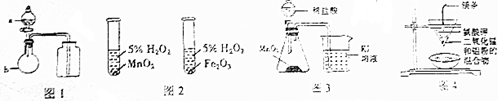
| A. | 用图1所示装置进行浓硫酸与亚硫酸钠的反应制取并收集SO2 | |
| B. | 用图2所示装置进行研究不同催化剂对反应速率的影响 | |
| C. | 用图3所示装置比较MnO2、Cl2、I2的氧化性 | |
| D. | 用图4所示装置可以制取金属锰 |
分析 A.实验室可以用浓硫酸和亚硫酸钠反应制取二氧化硫,利用强酸制取弱酸方法,二氧化硫密度大于空气且常温下和空气不反应,可以采用向上排空气法收集;
B.要研究不同催化剂对化学反应速率的影响,只有催化剂不同,其它条件必须完全相同;
C.浓盐酸和二氧化锰制取氯气必须需要加热条件;
D.可用铝热法冶炼锰.
解答 解:A.实验室可以用浓硫酸和亚硫酸钠反应制取二氧化硫,利用强酸制取弱酸方法,二氧化硫密度大于空气且常温下和空气不反应,可以采用向上排空气法收集,装置图符合条件,所以能实现目的,故A正确;
B.要研究不同催化剂对化学反应速率的影响,只有催化剂不同,其它条件必须完全相同,装置图符合条件,能实现目的,故B正确;
C.浓盐酸和二氧化锰制取氯气必须需要加热条件,所以该实验无法制取氯气,不能实现实验目的,故C错误;
D.铝比锰活泼,可用铝热法冶炼锰,故D正确;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及铝热反应、氧化性强弱比较、实验室制取和收集气体、催化剂对化学反应速率影响等知识点,明确实验原理及实验基本操作是解本题关键,易错选项是C.


科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中溶质微粒一定不带电,胶体中分解质微粒带有电荷 | |
| B. | 溶液呈电中性,胶体带电荷 | |
| C. | 胶体是比溶液更稳定的分散系 | |
| D. | 胶体是一种较稳定的分散系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体中N0的物质的量为0.01mol | |
| B. | 混合气体中N02的物质的量为0.02mol | |
| C. | 稀硝酸的浓度为0.045mol/L | |
| D. | 氢氧化钠溶液的浓度为0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +(n-1)H2O→n HOOCCH2CH(OH)COOH.
+(n-1)H2O→n HOOCCH2CH(OH)COOH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  和 和 | B. | 金刚石和石墨 | ||
| C. | H3C-O-CH3和CH3CH2OH | D. |  和 和 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 溶液A | 固体B | 气体C | |
| a | 稀硫酸 | Zn | Cl2 |
| b | 浓盐酸 | MnO2 | H2 |
| c | 稀硝酸 | Fe | Cl2 |
| d | 浓盐酸 | KMnO4 | H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com