
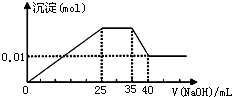
 有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:| A、原溶液一定不存在H+、Cu2+、CO32- |
| B、不能确定原溶液是否含有K+、NO3- |
| C、实验所加的NaOH的浓度为2mol?L-1 |
| D、原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n(NH4+)=1:1:2 |
| n |
| V |
| 0.05mol |
| 0.025L |


科目:高中化学 来源: 题型:
| A、物质失电子的反应为还原反应 |
| B、物质在变化中得到电子,此物质是还原剂 |
| C、发生电子转移的反应即是氧化还原反应 |
| D、发生化合价升降的反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生石灰、铁粉常用于食品干燥剂 |
| B、“地沟油”经过加工处理后可用来制肥皂 |
| C、抗酸药如小苏打可治疗因胃酸过多引起的消化不良 |
| D、以粮食为原料酿酒过程的变化包括粮食一淀粉一葡萄糖一乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若A为镁,X为氢气,则B一定是酸 |
| B、若B为H2O2,则X或Y中不可能有O2 |
| C、若A、B、X、Y均为化合物,该反应一定属于复分解反应 |
| D、若该反应为置换反应,A和X为单质,则A与X对应元素可能在同一周期,也可能在同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用太阳能分解水获得氢气 |
| B、用家用汽车代替公交车 |
| C、利用化石燃料制造燃料电池 |
| D、在农村推广建造沼气池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O3在反应中被氧化成O2 |
| B、反应中氧化产物O2与还原产物I2的物质的量之比为1:1 |
| C、H2O是氧化剂 |
| D、该反应中的还原产物是KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,氯气通入氢氧化钠溶液中反应:Cl2+2OH-=Cl-+ClO-+H2O |
| B、硫酸和氯化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| C、铁跟稀盐酸反应:Fe+2H+=H2↑+Fe3+ |
| D、碳酸钙和醋酸反应:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com