
| A. | 低温、低压 | B. | 低温、高压 | C. | 高温、高压 | D. | 高温、低压 |
科目:高中化学 来源: 题型:选择题
| A. | 混合物里三种物质反应时消耗盐酸的物质的量之比为1:1:3 | |
| B. | 反应后所得溶液中的Fe3+与的物质的量之比为1:3 | |
| C. | 混合物里FeO的物质的量无法确定,但Fe和Fe2O3的物质的量多 | |
| D. | 混合物里Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2是还原产物,且还原剂与氧化剂物质的量之比是2:3 | |
| B. | N2是氧化产物,且还原剂与氧化剂物质的量之比是2:3 | |
| C. | 每转移6mol电子就生成22.4LN2 | |
| D. | NH4Cl是氧化产物,且还原剂与氧化剂物质的量之比是2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子:1s22s22p63s23p63d10 | B. | B2-:1s22s22p6 | ||
| C. | C2+:1s22s22p6 | D. | D原子:1s22s22p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
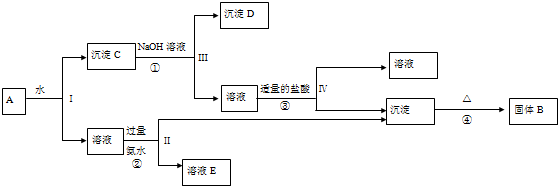
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
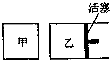 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,| A. | a>b | B. | a=b | C. | a<b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作及现象 | 结论 |
| A | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 溶液中含有NH4+ |
| B | 将浓硝酸滴入碳酸钠溶液中,然后将生成的气体直接通入硅酸钠溶液中,溶液变浑浊. | 酸性:硝酸>碳酸>硅酸 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,溶液变成蓝色 | 氧化性:I2>Cl2 |
| D | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
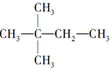 ,则A的结构简式为(CH3)3CCH=CH2.
,则A的结构简式为(CH3)3CCH=CH2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com